题目内容
【题目】下图能正确反映其对应操作中各种量的变化关系的是
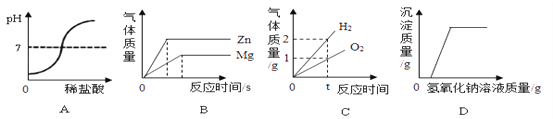
A. 在氢氧化钠溶液中加入一定量的稀盐酸,溶液pH的变化曲线
B. 将相同质量的Zn粉和Mg粉分别加入足量的稀盐酸中
C. 水的电解
D. 向盐酸和氯化铁混合溶液中加入过量的氢氧化钠溶液
【答案】D
【解析】A、氢氧化钠溶液显碱性,pH大于7,在氢氧化钠溶液中逐滴加入稀盐酸,pH值的变化是从大于7开始,错误;B、锌和稀盐酸反应生成氯化锌和氢气,镁和稀盐酸反应生成氯化镁和氢气,镁的金属活动性大于锌,镁和稀盐酸的反应速率比锌快,反应需要的时间短;反应的化学方程式及其质量关系为:Zn+2HCl═ZnCl2+H2↑,Mg+2HCl═MgCl2+H2↑,
65 2 24 2
由以上质量关系可知,完全反应后,镁和稀盐酸反应生成的氢气多,错误;C、电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2,质量比是8:1,错误;D、向盐酸和氯化铁混合溶液中加入过量的氢氧化钠溶液时,氢氧化钠先消耗稀盐酸,等盐酸完全消耗后,再消耗氯化铁反应生成氢氧化铁沉淀和氯化钠,正确。故选D。

练习册系列答案
相关题目