题目内容
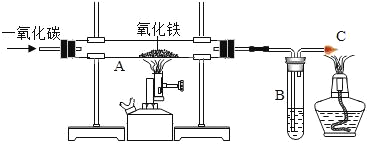
【题目】用一氧化碳冶炼氧化铁中的铁的步骤主要有:
①检查装置的气密性
②在硬质玻璃管中装入少量红棕色的氧化铁
③加热氧化铁
④通入一氧化碳,同时点燃尾气
⑤玻璃管冷却后停止通一氧化碳
⑥停止加热
⑦熄灭燃烧尾气的酒精灯
(1)上述实验的正确顺序是_____。
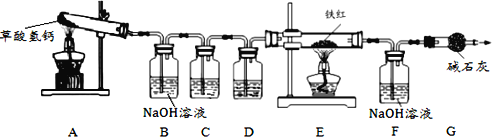
(2)硬质玻璃管A中看到红棕色固体已经完全变黑时,所发生化学反应的方程式是_____;为了检验生成的物质是否含有铁,还要进行简单实验,其操作和现象是_____,说明有铁生成了。
(3)根据实验需要,装置B中盛放的液体是_____,写出此过程发生的化学反应方程式:_____。
【答案】①②④③⑥⑤⑦ Fe2O3+3CO![]() 2Fe+3CO2 滴加稀盐酸,产生气泡 澄清的石灰水 CO2+Ca(OH)2=CaCO3↓+H2O
2Fe+3CO2 滴加稀盐酸,产生气泡 澄清的石灰水 CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
(1)先检查装置的气密性,在硬质玻璃管中装入少量红棕色的氧化铁,通入一氧化碳,同时点燃尾气,排出装置内的空气后,防止发生爆炸;停止加热,玻璃管冷却后停止通一氧化碳,防止生成的铁再次被氧化,熄灭燃烧尾气的酒精灯。
(2)一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管A中出现的现象是红棕色粉末逐渐变黑,反应的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2。铁能与稀盐酸反应生成氢气,检验生成的物质是否含有铁,可滴加稀盐酸,若产生气泡,说明生成了铁。
2Fe+3CO2。铁能与稀盐酸反应生成氢气,检验生成的物质是否含有铁,可滴加稀盐酸,若产生气泡,说明生成了铁。
(3)检验二氧化碳使用澄清的石灰水,装置B中盛放的液体是澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案【题目】化学实验过程经常会产生一定量的废液,经过无害化处理可有效防止水体污染。在一次实验课上,兴趣小组的同学们完成了NaOH溶液和Na2CO3溶液的鉴别,并对废液成分展开探究。
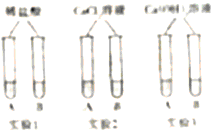
活动一
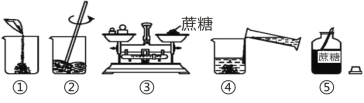
通过小组合作,同学们完成了右图所示的三组小实验。实验中生成白色沉淀的化学方程式是____________________(写一个)。
活动二
小雪将六支试管中的剩余物倒入一个洁净的大烧杯中(如下图), 充分搅拌、静置。观察到杯内上层是无色溶液,下层有白色沉淀。由此可以确定:上层溶液中一定不含有的离子是__________________、以及一定含有的离子。小组同学对上层溶液中还可能含有的离子进行了如下探究。![]()
(提出问题)上层溶液中还可能含有什么离子?
(猜想与假设)上层溶液中还可能含有OH-、CO32-、Ca2+中的一种或几种。
(进行实验)
实验步骤 | 实验现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液②继续滴加稀盐酸 | ①溶液变红 ②产生气泡 | ①有OH- ②有CO32-、无Ca2+ |
方案二 | 取少量溶液于试管中,____________(指示剂除外) | ①____________ ②___________ | ①有CO32-、无Ca2+ ②有OH- |
(反思与评价)
(1)小明同学对方案一提出质疑, 他的理由是________________________。
(2)经过综合分析,最终确定上层溶液中肯定存在的离子有______________________。
(3)将烧杯内物质过滤,滤渣回收,向滤液中加入适量_______________________进行处理后再排放。