题目内容
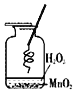
【题目】用氯酸钾和二氧化锰的混合物16g加热制取氧气,至不再产生气体,冷却后称量剩余固体的质量为11.2g。(1)生成氧气多少克_______?
(2)原混合物中有多少克氯酸钾_______?
【答案】4.8g 12.25g
【解析】
氯酸钾在二氧化锰催化下受热分解生成氯化钾和氧气,反应中二氧化锰为催化剂其质量在变化前后质量不变;由于反应产生气体氧气,根据质量守恒定律,完全反应前后固体物质的质量差即为放出氧气的质量;利用反应得到氧气的质量,根据反应的化学方程式,可计算参加反应氯酸钾质量。
(1)氯酸钾在二氧化锰催化下受热分解生成氯化钾和氧气,反应中二氧化锰为催化剂其质量在变化前后质量不变;所以可知反应前后固体减轻的质量是氧气的质量,则是16g-11.2g=4.8g;
(2)根据设原混合物中KClO3质量为x,
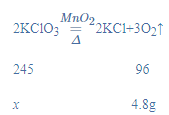
![]()
x=12.25g。

【题目】实验室有5种白色固体,老师让化学实验小组同学鉴别这些固体.
(1)调查研究
①5种白色固体分别是:NaOH、Na2CO3、CuSO4、Ca(OH)2和NaHCO3.
②查阅资料:小组同学查阅了NaOH、Na2CO3和NaHCO3的一些性质.
性质 | NaOH | Na2CO3 | NaHCO3 |
溶解性 | 20℃时溶解度109g | 20℃时溶解度21.5g 溶解时放热 | 20℃时溶解度9.6g溶解时放热 |
加热 | 不分解 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
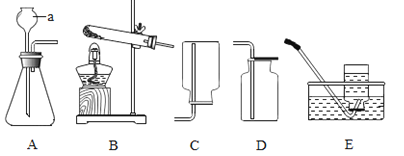
(2)实验探究:同学们的探究报告如下,请你帮助完成.
实验步骤 | 实验现象 | 实验结论 | |
第一步:在5支试管中分别放入少量的5种白色固体, 分别标上A、B、C、D、E,然后依次加入一定量的水并振荡. | A、C、D的溶液为无色;B的溶液为浑浊;E的溶液呈蓝色. | B是_____ E是_____ | |
第二步:向上述A、C、D溶液中分别滴加无色的酚酞溶液. | 三支试管中的酚酞溶液均变红. | 结论: _____ | |
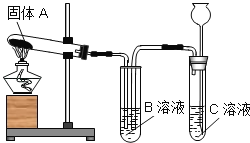
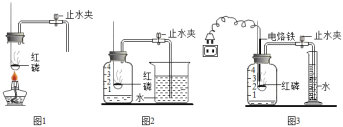
第三步:依据如图装置,对A、B、C进行实验. |
| ||
①加热固体A | B溶液无明显现象. | A是Na2CO3 | |
②待①停止加热后,通过长颈漏斗向C溶液中加入稀盐酸 | C溶液中有气泡产生,B溶液中有气泡逸出并有白色沉淀生成. | B溶液中发生反应的化学方程式为_____ | |
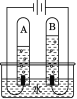
第四步:依据如图装置,对B、C进行实验. |
| 被加热的试管口有无色液滴生成,B溶液中有气泡逸出且溶液变浑浊. | C是_____ 利用排除法得出:D是NaOH |
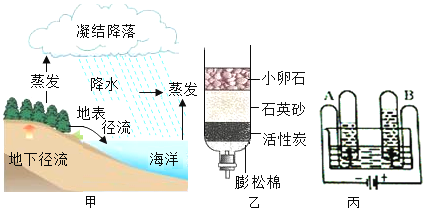
(3)实验反思:老师引导同学们讨论了上述实验探究过程,进行全面反思,发现实验结论仍有不确定性,不能确定的物质是_____(填化学式);请用物理方法继续鉴别.
实验步骤 | 实验现象和结论 |
_____ | _____ |