题目内容
【题目】请回答下列有关水的问题:
(1)自来水生产过程中先用_____的方法除去水中不溶性杂质,再进行吸附、消毒等。
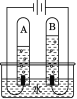
(2)如图是电解水的实验装置。在实验过程中,试管A中产生的气体是_________,该实验可以得出的结论是____________。
(3)下列各种水中,属于纯净物的是________。
A.自来水 B.冰水混合物 C.河水 D.硬水
(4)检查河水是硬水还是软水,可用的物质是____________;
(5)生活中硬水软化的方法是____________;实验室硬水软化的方法是____________;
(6)活性炭能除去洲河水中有颜色、有异味的物质,这是利用活性炭的_______性;
【答案】过滤 氢气 水是由氢、氧两种元素组成的 B 肥皂水 煮沸 蒸馏 吸附
【解析】
(1)自来水生产过程中先用过滤的方法除去水中的不溶性杂质;
(2)由电解水的简易装置示意图可知,A试管中收集的气体较多是氢气,应是电源的负极产生的气体,B试管中气体体积较少,为氧气,电解水生成了氢气和氧气说明水由氢元素和氧元素组成;
(3)A、自来水的主要成分是水,还含有一些溶于水的物质,属于混合物;
B、冰水混合物中只有水这一种物质,属于纯净物;
C、河水的主要成分是水,还含有一些溶于水的物质,属于混合物;
D、硬水中除了水以外,还含有较多的可溶性钙、镁离子化合物,属于混合物;
(4)区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;
(5)降低水的硬度的方法是:在生活中是煮沸,在实验室中是蒸馏;
(6)活性炭有吸附作用,可以吸附一些色素、异味等。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量见表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 6.0 | 2.2 | 2.6 | 0.7 |
反应后质量/g | 待测 | 4.0 | 3.6 | 0.7 |
关于这四种物质,下列说法正确的是( )
A. 甲、乙是反应物,丙是生成物 B. 丁定是该反应的催化剂
C. 参加反应的甲的质量为![]() D. 甲一定是化合物
D. 甲一定是化合物