题目内容
【题目】铜镁合金常用做飞机天线等导电材料。欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金10g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
次 数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
剩余固体质量/g | 8.5 | 7 | 6.6 | 6.6 |
(1)铜镁合金中铜的质量分数。
(2)求所加稀硫酸中溶质的质量分数。(写出计算过程)
【答案】66%;12.25%
【解析】
镁和稀硫酸反应生成硫酸镁和氢气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算。
(1)最终剩余的6.6g是不能和稀硫酸反应的铜的质量,镁合金中铜的质量分数为:![]() ×100%=66%;
×100%=66%;
(2)设第一次加入的50g稀硫酸中硫酸质量为x,第一次反应的镁质量为:10g-8.5g=1.5g,

![]()
x=6.125g;
所加稀硫酸中溶质的质量分数为:![]() ×100%=12.25%。
×100%=12.25%。

【题目】活动小组为测定由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该固体混合物各20g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如下表:
组别 | 第1组 | 第2组 | 第3组 |
稀硫酸质量/g | 50 | 100 | 150 |
剩余固体的质量/g | 10.0 | 4.0 | 4.0 |
根据实验及有关数据进行分析与计算:
(1)第1组实验中_____________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)完全反应。
(2)样品中氧化铜的质量分数是__________g。
(3)根据第1组实验数据计算所用的稀硫酸溶质的质量分数__________(写出计算过程)。
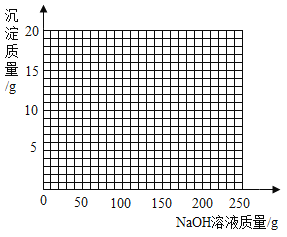
(4)若将第2组实验后的混合物过滤,在滤液中滴加10%的NaOH溶液,请画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图__________。