题目内容
【题目】如图为某品牌过氧化氢溶液说明书,,用该品牌过氧化氢溶液配制600g10%的过氧化氢溶液用于消毒,请回答下列问题:

(1)溶质(H2O2)的相对分子质量_____________。
(2)溶质(H2O2)中氢、氧元素质量比为_____________。
(3)600g10%的过氧化氢溶液中含有_____________g溶质,配置时需要加入__________g水进行稀释。
【答案】 34 1:16 60; 400
【解析】
(1)过氧化氢的相对分子质量为2+16×2=34;
(2)H2O2中氢、氧元素质量比为2:(16×2)=1:16;
(3)600g10%的过氧化氢溶液中含有溶质过氧化氢的质量为600g×10%=60g;
设配制过程中加入水的质量为x,则30%的过氧化氢的质量为600-x,则(600-x)×30%=60g,解得x=400g;、
答:过氧化氢的相对分子质量为34;H2O2中氢、氧元素质量比为1:16; 600g10%的过氧化氢溶液中含有溶质过氧化氢的质量为60g;配制过程中加入水的质量为400g。

【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是
物质 | a | b | c | d |
反应前质量(g) | 10 | 10 | 10 | 2 |
反应后质量(g) | 待测 | 2 | 21 | 2 |
A.该反应是化合反应,d可能是催化剂
B.a、b两种物质中元素种类一定与c物质中元素种类相同
C.b物质可能是单质
D.反应后a物质的质量为3g
【题目】某校课外活动小组为了探究化学变化中的质量守恒定律,做了两个探究实验:
问题:研究化学变化中物质质量的变化规律
(1)我的假设:物质发生化学反应前后,其总质量___________________。
(2)我的探究:
实验编号 | 实验一 | 实验二 |
实验装置 |
|
|
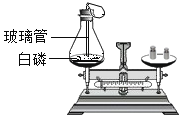
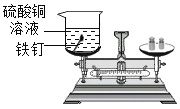
实验操作 | 将如上图所示装置放在天平上称量后取下,将玻璃管烧至红热后,迅速插入锥形瓶中,点燃白磷,并塞紧瓶塞,待反应结束,冷却后,放回托盘天平观察天平。 | 将铁钉和盛有硫酸铜溶液的烧杯一起放在托盘天平上称量后取下,将铁钉浸泡在硫酸铜溶液中一段时间待反应不再继续,再放回托盘天平上,观察天平。 |
化学方程式 | ________ | ________ |
反应前后天平是否平衡 | ________ | __________ |
(3)我的结论:_______________________________________________。
(4)我的解释:_______________________________________________。
【题目】某校化学兴趣小组的同学在实验室整理化学药品时,发现一瓶金属铬。为了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,他们进行了如下探究活动:
(查阅资料)铬(Cr)是银白色金属,在空气中其表面能形成致密的氧化膜。
(提出假设)考虑到铝的活动性比铜强,提出了以下三种假设:
假设①:![]() ;
;
假设②:![]() ;
;
假设③:![]() 。
。
(实验过程)取大小相同的Cr、Cu、Al三种金属薄片,用砂纸打磨光亮后,分别放入三支试管中,再分别加入等体积![]() 的稀硫酸。
的稀硫酸。
(实验现象)
金属 | Cr | Cu | Al |
实验现象 | 铬片表面产生气泡缓慢 | 铜片表面无明显变化 | 铝片表面产生气泡较快 |
(实验结论)假设___________成立(填序号)。
(问题与反思)
(1)由上述结论可知,铬可以与硫酸铜溶液发生反应。请写出该反应的化学方程式:________(已知在该反应的生成物中铬元素显![]() 价)。
价)。
(2)小丽提出,按上述实验操作,用硫酸铜溶液代替稀硫酸也能得出三种金属的活动性顺序,你认为_________(填“可行”或“不可行”),理由是________。