题目内容
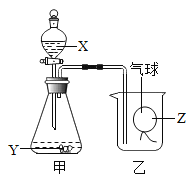
【题目】金属在日常生活中有着广泛的用途。常见金属的活动性顺序如图

请回答下面问题:
(1)金属活动性顺序表中的X是_____元素。(填元素符号)
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为_____
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图2所示。图中B点溶液中含有的溶质有_____(填化学式)
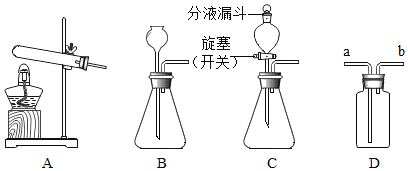
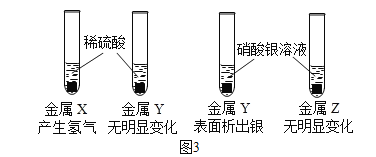
(4)为比较三种金属活动性大小,进行如图3实验。三种金属的活动性顺序是_____
(5)非金属单质也具有类似金属与盐溶液之间发生置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐酸溶液中置换出来,如在溶液中可发生下列反应:
Cl2+2NaBr=2NaCl+Br2、I2+Na2S=2NaI+S↓、Br2+2KI=2KBr+I2
由此判断S、Cl2、I2、Br2四种单质中非金属活动性最强的是_____
【答案】Hg 2Al+3CuSO4=Al2(SO4)3+3Cu Zn(NO3)2、Cu(NO3)2 X>Y>Z Cl2
【解析】
(1)金属活动性顺序表中的X是汞元素,符号为:Hg;
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,则铝与硫酸铜反应生成硫酸铝和铜,该反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu;
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,则锌首先与硝酸银反应,到达B点银全部被置换出来,图中B点溶液中含有的溶质有硝酸锌和硝酸铜;
(4)根据图3实验可以看出,X产生氢气,Y无变化,说明X的活动性强于Y,Y能置换出银,二Z不能,说明Y的活动性强于银,故三种金属的活动性顺序是:X>Y>Z;
(5)根据Cl2+2NaBr=2NaCl+Br2、氯气的活动性强于溴,I2+Na2S=2NaI+S↓、碘的活动性强于硫,Br2+2KI=2KBr+I2溴的活动性强于碘,即活动性为:Cl2>Br2>I2>S,由此判断S、Cl2、I2、Br2四种单质中非金属活动性最强的是 Cl2。

 名校课堂系列答案
名校课堂系列答案【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
温度(℃) | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
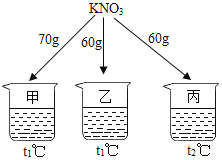
A. 甲、乙混合后为t1℃的不饱和溶液
B. 乙升温至t2℃,溶液质量增加
C. 乙、丙溶液中溶质质量相等
D. 丙降温至t1℃,有晶体析出