题目内容
【题目】明明同学用如图装置进行实验,开始时气球沉于烧杯底部,气球内气体Z为单质(气球质量忽略不计)。打开分液漏斗活塞后,过一会儿气球从烧杯底部慢慢浮起,最后悬于烧杯口。实验过程中没有产生有毒气体。请回答:
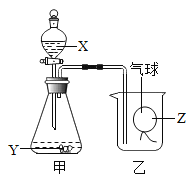
(1)写出制取Z的化学方程式_____。
(2)写出X与Y反应的化学方程式_____。
【答案】2H2O2 ![]() 2H2O + O2↑(答案合理均可) 2HCl + CaCO3 = CaCl2 + H2O + CO2
2H2O + O2↑(答案合理均可) 2HCl + CaCO3 = CaCl2 + H2O + CO2
【解析】
气球内的气体是单质,且X和Y产生的气体后气球浮起,说明产生的气体的密度大于气球内气体的密度,故Z可以是氧气,产生的气体可以是二氧化碳,故X是稀盐酸,Y是碳酸钙,
(1)过氧化氢在二氧化锰的催化作用下反应生成水和氧气,
故填:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳,
故填:2HCl+CaCO3═CaCl2+H2O+CO2↑.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目