��Ŀ����
����Ŀ��ʵ����ѧͬѧ��չ���ֽⷴӦ�о���ѧϰ������������о���ѧϰ˼·��
����ϰ���ɣ����и������ʼ���ܷ�Ӧ��д���ۡ��ܷ�Ӧ�Ļ�ѧ����ʽ��
������������Һ������ ��̼������Һ������
������ͭ��Һ������������Һ_____��
��̼������Һ���Ȼ�����Һ_____��
���о����ۣ�������ӦΪʲô�ܹ�����������Ϊ��Щ��Ӧ���к�����������������ӣ��������H+��OH����������H+��CO32����������_____��������_____��
���������磩����һ����˳��������Щ���ӣ��Ϳ����γ�һ��������ʽ���������У��ö�����������Щ����������������������ɳ����������ˮ������Ca2+��SO42����NH4+���뽫��������������ʵ���______��_____��_____���У�ʹ���γ�һ����Ϊ�����ĸ��ֽⷴӦ���磮
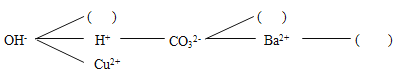
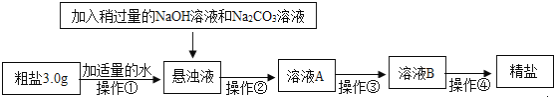
����չ���ã�ͨ���γɵ����磬�����жϻ�������ܷ棬�������ʵļ����������ʵij��ӵȣ�����������Һ��������泥����Լ���_____����д��ѧʽ����ȥ����泥�
���𰸡�2NaOH+CuSO4=Na2SO4+Cu��OH��2�� Na2CO3+BaCl2=BaCO3��+2 NaCl Cu2+��OH�� Ba2+��CO32�� NH4+ Ca2+ SO42�� NaOH
��������
��������ε�֪ʶ������⣬���ݸ��ֽⷴӦ���������ɳ��������������ˮ���ֽⷴӦ���ܷ�����գ���ֽⷴӦ������Ca2+��SO42����NH4+�����Խ����
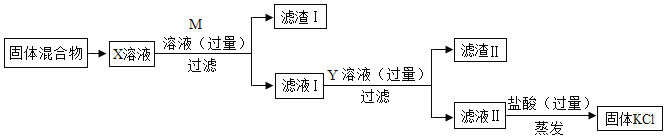
[��ϰ����]����ͭ��Һ������������Һ��Ӧ����������ͭ�����������ƣ��ʢ۴𰸣�2NaOH+CuSO4=Na2SO4+Cu��OH��2����
̼������Һ���Ȼ�����Һ��Ӧ����̼�ᱵ���Ȼ��ƣ��ʢܴ𰸣�Na2CO3+BaCl2=BaCO3��+2 NaCl��
[�о�����]����������������������ɳ����������ˮ���ֽⷴӦ�Ϳɷ�����������Cu2+��OH����������Ba2+��CO32����
[��������]��������������NH4+��OH���ܲ���������ˮ��������������������Ӳ�����ɫ������̼�������������Ӳ�����ɫ�������ʴ𰸣�NH4+��Ca2+��SO42����
[��չ����]��ȥ�������е������ʵ���dz�ȥ笠����ӣ������и��ֽⷴӦ����֪ѡ�ü�ֲ�����������������ѡ�������ƣ��ʴ𰸣�NaOH