题目内容
【题目】小明同学在学校实验室找到一瓶没有标注溶质的质量分数的盐酸,为确定盐酸中溶质的质量分数,现取10.0g碳酸钙于烧杯中,滴入20.0g盐酸时恰好完全反应,反应后得到25.6g溶液(注:忽略CO2的溶解性)。(该反应的化学方程式为![]() )
)
(1)产生的CO2的质量是 。
(2)盐酸中溶质的质量分数是多少?
【答案】(1)4.4g。(2)36.5%。
【解析】
(1)由题意,碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,不考虑二氧化碳的溶解性,反应生成的二氧化碳逸出,物质的总质量减小,减小的质量即为生成的二氧化碳的质量,则产生的CO2的质量是10.0g+20.0g-25.6g=4.4g。
(2)设生成4.4g二氧化碳消耗氯化氢的质量为x,则有:
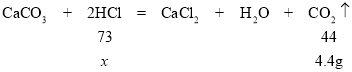
由![]() 解得x=7.3g
解得x=7.3g
则盐酸中溶质的质量分数是![]()
答:盐酸中溶质的质量分数是36.5%。

练习册系列答案
相关题目
【题目】下列对比实验的设计不能到达相应实验目的的是
选项 | A | B | C | D |
实验 设计 |
|
|
|
|
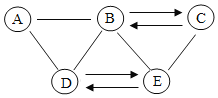
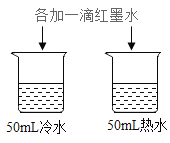
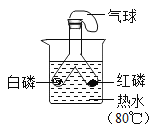
实验 目的 | 探究温度对分子运 动快慢的影响 | 探究燃烧的条件 | 探究铁、镁金属活 动性强弱 | 探 究CO2与 NaOH 溶液能否发生反应 |
A.AB.BC.CD.D