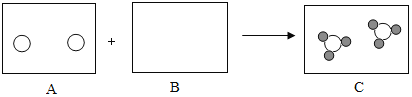
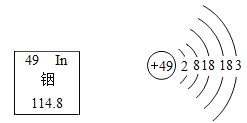题目内容
【题目】(1)金属钛(Ti)具有熔点高、密度小、抗腐蚀、易于加工等优良性能,被誉为“未来的金属”。工业上以钛酸亚铁(FeTiO3)等原料经过一系列反应制备纳米TiO2和钛,主要生产过程如下:(其他产物已略去)
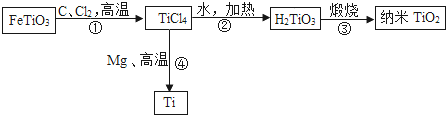
①反应①生成两种氯化物和一种有毒的氧化物气体,该气体的化学式是________ 。
②反应③中另一种生成物是________________。
③反应①②③④中属于置换反应的是________ (填序号)。
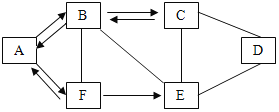
(2)已知A、B、C、D、E分别为初中化学常见的物质,其中A、B、D、E分别为氧化物、酸、碱、盐中的一种,A是人体胃液中的酸,C是实验室中最常用的溶剂,D广泛用于玻璃、造纸、纺织和洗涤剂的生产,E与C反应,能使紫色石蕊溶液变红。它们的部分反应和转化关系如图所示。(“一”表示两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物或生成物及反应条件)
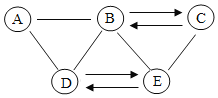
①D的俗名为_____;其水溶液的pH值_____________7(填“>”、“=”或“<”)
②B是实验室的常见物质,A与B能反应的原因是_____,A与B反应的基本类型是_____。
③写出B与D反应的化学方程式___________________。
【答案】CO H2O ④ 纯碱(或苏打) > ![]() 复分解反应
复分解反应 ![]()
【解析】
(1)①反应①的反应物有FeTiO3、C和Cl2,根据反应前后元素种类守恒,以及生成两种氯化物和一种有毒的氧化物气体,可得有毒的气态氧化物就是一氧化碳,化学式是CO。故填:CO。
②根据反应前后元素种类守恒,反应③H2TiO3煅烧分解后,生成TiO2和另一种物质水。故填:H2O。
③一种单质与一种化合物反应生成另一种单质和另一种化合物的反应叫做置换反应,反应①有三种反应物,不符合置换反应的概念;反应②的反应物是氯化钛和水两种化合物,不符合置换反应的概念;反应③属于分解反应;只有反应④(有单质镁与四氯化钛参加反应生成单质钛和氯化镁)属于置换反应。故填:④。
(2)已知A、B、C、D、E分别为初中化学常见的物质, A是人体胃液中的酸即盐酸,C是实验室中最常用的溶剂水,D广泛用于玻璃、造纸、纺织和洗涤剂的生产,所以D是碳酸钠,其中A、B、D、E分别为氧化物、酸、碱、盐中的一种,A、D分别是酸和盐,所以B、E分别是碱和氧化物中的一种,根据框图可知,D碳酸钠可以与B反应,所以B是一种碱如氢氧化钙,碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,E是一种氧化物,且能与碳酸钠相互转化,所以E是二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠与盐酸反应生成二氧化碳,符合框图DE可以相互转化,二氧化碳与C(水)反应生成的碳酸能使紫色石蕊溶液变红。
①由以上分析可知D是碳酸钠,俗名为纯碱或苏打;其水溶液显碱性,pH值>7。故填:纯碱(或苏打);>。
②由以上分析B是氢氧化钙,A是稀盐酸,AB能反应的原因是酸中的氢离子和碱中的氢氧根离子反应结合成水分子,A与B反应即酸碱中和反应符合双交换价不变的特点,所以该反应的基本反应类型属于复分解反应。故填:![]() ;复分解反应。
;复分解反应。
③由以上分析可得,B氢氧化钙与D碳酸钠反应生成碳酸钙沉淀与氢氧化钠,反应的化学方程式![]() 。故填:
。故填:![]() 。
。

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】研究金属的腐蚀对资源的利用和保护意义重大.

(1)为了探究铁锈蚀的条件,进行如图![]() 所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.通过实验发现:铁锈蚀是铁与______________发生化学反应的过程.
所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.通过实验发现:铁锈蚀是铁与______________发生化学反应的过程.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
(提出问题)铁锈蚀速率与哪些因素有关.
(查阅资料)①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
(猜想)铁的锈蚀速率与下列因素有关:
①反应时的温度;②氧气的含量;③水溶液的导电性.
(实验)每次取两套如图![]() 所示的装置,编号为
所示的装置,编号为![]() 、
、![]() 向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
①温度 | 装置 | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间 | 锈蚀的速率 |
②氧气含量 | ______________. | ___________. | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快. |
③水溶液的导电性 | 在相同温度下,装置 | 两套装置中铁钉均锈;且U型管中液面均由b处上升至a处,则所需时间 | __________. |
(3)若将两根铁钉分别放入两支试管中,在一支试管中加入稀硫酸,另一支试管中加入稀盐酸,观察到两支试管内均有大量气泡产生,铁钉逐渐溶解,在酸溶液中被快速腐蚀.
(反思与提高)
根据该探究实验以及你所学的知识,判断下列说法正确的是________(填序号).
a.金属的腐蚀是指金属单质与其它物质发生化学反应的过程
b.金属越活泼,就越容易被锈蚀
c.金属腐蚀不一定要有氧气参加.
【题目】(1)三四两月,桃花李花竞相开放,植物长出嫩嫩绿芽,空气清新。花海飘香,使人流连忘返。
①树林中富含抗氧化防衰老的负氧离子。一种负氧离子(O2-)的一个原子团是由一个O2分子俘获了空气中一个自由电子形成的微粒,每个O2-中共含有_____个电子。
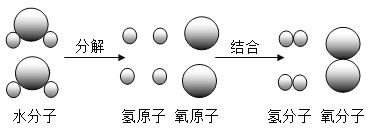
②鲜花的香味在空气中扩散,是大量的带有香味的分子_____的结果。
③培育鲜花的某种营养液呈蓝色,可能由KNO3、Ca(NO3)2、CuCl2中的一种或几种物质配制而成,其中Ca、N的元素质量比为1:1,则该营养液中含有_____种溶质。从均衡植物所需营养元素的角度分析,营养液中还需补充_____(填元素符号)。
(2)分析处理图表中的信息是学习化学的一种重要方法。
如表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
①40℃时,氯化钠的溶解度为________g。
②在20℃时,将100g的水加入30g碳酸钠中,充分搅拌后得到的是________(填“饱和溶液”或“不饱和溶液”)
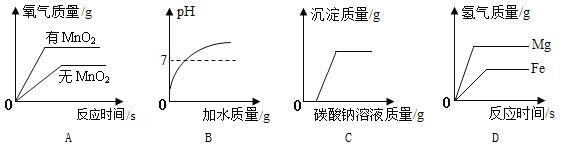
(3)根据所学知识回答下列与金属材料有关的问题。
将过量的稀盐酸加入一定量的铁、铜混合物中,反应后溶液中溶质有________种。如图是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示不正确的是________(填标号)。