题目内容
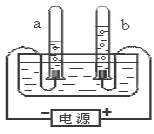
【题目】某学习小组利用下图装置,对空气成分的探究进行了如下实验:(提示:通常条件下,白磷与氢氧化钠溶液不反应。二氧化碳与氢氧化钠溶液反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O)
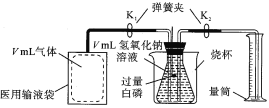
(1)先检查装置的气密性,装入试剂,在医用输液袋中装入VmL空气,连接装置。
(2)打开弹簧夹K1.K2,缓慢将袋中的空气全部排出。读出量筒中液体体积为V1 mL
(3)关闭弹簧夹K1.K2,再向烧杯中加入热水,观察到白磷燃烧。
(4)待装置冷却至室温,打开K2,读出量筒中液体体积为V2 mL。
以下说法正确的是( )
A. 步骤(3)中加入热水的作用是吸收五氧化二磷,防止污染空气
B. 根据以上数据分析可得氧气的体积分数为:(V1-V2)/V1×100%
C. V2 mL是空气中已反应的氧气之外的气体的总体积
D. 若白磷的量不足,会导致V2的读数偏大
【答案】D
【解析】
A、步骤(3)中加入热水的作用是提供热量,使白磷的温度达到着火点,白磷迅速燃烧,故A错误;
B、在步骤(2)实验中锥形瓶中氢氧化钠溶液吸收气体中的二氧化碳,减少的液体体积是二氧化碳的体积,二氧化碳的体积=V-V1;在步骤(4)中量筒中液体体积为V2mL,其数值等于己反应的氧气和二氧化碳之外的气体总体积,所以![]() ,
,![]() ,
,![]() ,氧气的体积分数=
,氧气的体积分数=![]() ,故B错误;
,故B错误;
C、V2 mL是空气中已反应的氧气和二氧化碳之外的气体的总体积,故C错误;
D、若白磷的量不足,氧气不能完全消耗,会导致V2的读数偏大,故D正确。故选D。

 阅读快车系列答案
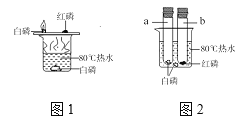
阅读快车系列答案【题目】(问题情景)在课外活动中,小斌按照课本实验(见图1)探究分子的运动时,闻到了刺激性的氨味,于是,小斌在老师的指导下,设计了如图2的实验装置,进行同样的实验,结果不再有刺激性的氨味,并且快速出现实验现象,得到了和课本实验同样的结论。
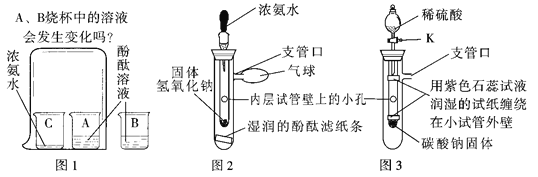
(资料在线)①Na2CO3+H2SO4 ——- Na2SO4 + H2O + CO2 ②氢氧化钠固体溶于水时放热
(实验探究与结论)小斌用图2装置进行实验。
(1)滴入少量浓氨水后,湿润的酚酞滤纸条发生的变化是_____。从分子运动的角度分析,此现象可说明的结论是_______;
(2)和课本实验比较,小帅同学改进后的装置的优点是_________________
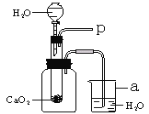
(思维拓展)小媚受小斌实验的启发,将图2装置进一步改装成图3装置,用于验证二氧化碳的性质。
①打开活塞K滴入稀硫酸后,两条用紫色石蕊试液润湿的试纸线变红色的是_______,小媚这一现象说明二氧化碳具有的物理性质是_______。
②氨气可以由碳酸氢铵受热分解产生,请写出反应的化学表达式是_____________。
某同学用含碳酸氢铵的化肥制取收集氨气,
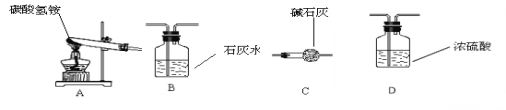
若将装置A、C、D依次连接,加入25g化肥样品,加热至A中固体质量不再改变。她称量装置D的质量如表:
实验前D装置的质量 | 150g |
实验后D装置的质量 | 153.4g |
③由此分析得知:反应中产生氨气的质量_________g。
④通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮元素的质量分数为__________________。
⑤请计算此化肥中碳酸氢铵的质量分数为 _____________。