题目内容
【题目】小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究。
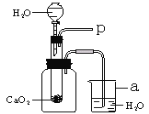
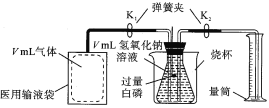
(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如如图所示的装置进行实验。实验过程如下:打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是_______。由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是__________,试解释仪器a中导气管口产生气泡可能的原理__________。
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物。开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2。请解释小强否定原假设建立新假设的理由:_____________。
(3)请写出过氧化钙与水反应的化学方程式:___________。
(4)生铁和钢都是铁的合金,由于________不同,二者性能不同。
【答案】氧气 向鱼塘中增加氧气 过氧化钙与水反应放出热量,使集气瓶内气体受热膨胀,从导管口逸出。 反应前有氢元素,反应后也必须有氢元素 2CaO2+2H2O===2Ca(OH)2+O2↑ 含碳量不同
【解析】
(1)能使带火星的木条复燃的气体是氧气,故填氧气;过氧化钙与水生成氧气,可以增加鱼塘中的含氧量,故填向鱼塘中增加氧气;仪器a中导气管口产生气泡是因为过氧化钙与水反应放出热量,使集气瓶内气体受热膨胀,从导管口逸出,故填过氧化钙与水反应放出热量,使集气瓶内气体受热膨胀,从导管口逸出。
(2)过氧化钙与水反应,水中含有氢元素,生成物中一定含有氢元素,故填反应前有氢元素,反应后也必须有氢元素。
(3)过氧化钙与水反应生成氢氧化钙和氧气,故化学方程式写为:2CaO2+2H2O=2Ca(OH)2+O2↑。
(4)生铁含碳量在2%~4.3%之间,钢含碳量在0.03%~2%之间,物质的组成影响物质的性质,所以两种物质的性能不同,故填含碳量不同。

【题目】化学离不开实验,以下是实验室部分仪器或装置如图所示,请回答下列问题:

(1)B仪器的名称是_________。
(2)若要组装一套二氧化碳的发生装置,可选择图中的________________(填仪器下方的字母),写出实验室制二氧化碳的化学符号表达式为_______,该发生装置还可以制取的气体是_____(填一种)。
(3)若用氯酸钾制取氧气,发生装置除需A、C、E以外,还需要另外增加的仪器是_____。写出用氯酸钾制取氧气的化学符号表达式_______。
(4)CO2能与Ca(OH)2发生反应。
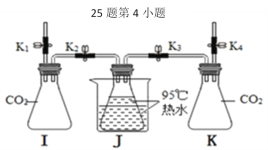
[实验过程]检查装置气密性,如图所示连接
好装置,进行实验。
序号 | 操作步骤 | 实验现象 |
Ⅰ | 打开弹簧夹K1,关闭弹簧夹K2、K3、K4。将20mL水注入锥形瓶I中,关闭弹簧夹K1,振荡瓶J,打开弹簧夹K2。 | 无明显现象 |
Ⅱ | 关闭弹簧夹K2,打开弹簧夹K4,将20mLCa(OH)2溶液注入锥形瓶K中,关闭弹簧夹K4,振荡瓶J,打开弹簧夹K3。 | 锥形瓶J中的热水剧烈沸腾 |
[实验分析]锥形瓶J的热水剧烈沸腾的原因是_________________。
[实验反思]有观点认为只需要进行实验操作Ⅱ,即可说明CO2与Ca(OH)2发生反应.你对其的看法是_______(选填“赞同”或“不赞同”),理由是________________。