题目内容
【题目】过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,某实验小组在实验室用两种方法制取CaO2。
【查阅资料】
从溶液中制得的过氧化钙含有结晶水,其结晶水合物化学式为CaO2·8H2O,在140~200℃脱水干燥,即得过氧化钙成品。加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气。过氧化钙与水反应生成氢氧化钙和氧气。
【进行实验】
甲组:由鸡蛋壳(含碳酸钙高达90%)为原料最终反应制得,其制备流程如图所示,其中鸡蛋壳的预处理主要是除去碳酸钙以外的大部分杂质。
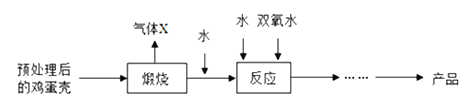
(1)气体X是__________,两次加水发生的都是化合反应,写出相关反应方程式__________,______ CaO2·8H2O,实际获得的产品不纯,主要含有的固体杂质是____________。
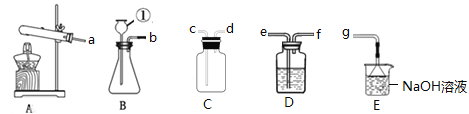
乙组:由氨气、双氧水、氯化钙为原料,制得CaO2·8H2O沉淀,同时产生副产品氯化氢,反应装置如图2所示。

(2)装置A加热的是熟石灰和硫酸铵,写出该反应的化学方程式_____________________。
(3)制取CaO2·8H2O的化学方程式:CaCl2+H2O2+2NH3·H2O+6H2OCaO2·8H2O+2Y。则Y的化学式________,该反应一般在0~5℃的低温下进行,温度不能过高的原因是_______________。
【定性测定】
(4)产品性质测定:甲组取产品充分加热,可用_________ 检验产生的气体。乙组取产品加水,滴入无色酚酞溶液,酚酞变红,说明产品加水后生成碱性物质。若需得到同样的结论,甲组______(填“能”或“不能”)采用与乙组相同的方法。
【定量测定】
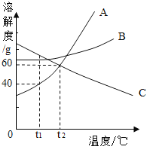
(5)2.76g CaO2·8H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140℃时完全脱水,杂质受热不分解)如图3所示。
① 试确定CaO2·8H2O样品中结晶水的质量=______g。
② 该样品中CaO2·8H2O的质量分数。(写出计算过程)_________
【交流讨论】
(6)对于上述两种制取CaO2·8H2O的方法有关评价合理的是_________(填序号)。
A.理论上甲组反应的原子利用率达100%,符合绿色化学理念
B.在原料充分转化的前提下,甲组的CaO2·8H2O沉淀过滤后不用洗涤,操作简便
C.乙组产生的副产品氯化氢可能会影响CaO2的产率
【答案】 CO2 CaO+H2O=Ca(OH)2 Ca(OH)2+H2O2+6H2O= CaO2·8H2O Ca(OH)2 Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O NH4Cl 防止NH3·H2O挥发,提高原料利用率 带火星的木条 不能 1.44g 78.3% ABC
CaCl2+2NH3↑+2H2O NH4Cl 防止NH3·H2O挥发,提高原料利用率 带火星的木条 不能 1.44g 78.3% ABC
【解析】(1)根据碳酸钙在高温的条件下分解生成氧化钙和二氧化碳解答;根据两次加水发生的都是化合反应,其一是氧化钙和水反应生成氢氧化钙,其二是氧化钙和过氧化氢以及水反应生成 CaO2·8H2O解答;根据过程中氧化钙遇到了水生成氢氧化钙解答;(2)根据熟石灰和硫酸铵在加热的条件下生成硫酸钙和氨气以及水解答;(3)根据质量守恒定律分析解答;根据过程中加入了氨水,氨水是氨气溶解于水形成的溶液,所以温度升高会导致气体溶解度降低而挥发出来解答;(4)根据信息提示为“加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气”解答;根据信息提示“过氧化钙与水反应生成氢氧化钙和氧气”,生成物为碱性的氢氧化钙,所以滴入无色酚酞溶液,酚酞变红。由于甲组加热后生成了氧化钙,而氧化钙遇到无色酚酞溶液,能和水反应得到碱性的氢氧化钙,使酚酞变红解答;(5)根据反应的化学方程式计算解答;(6)根据题中信息解答。(1)由于气体X是高温煅烧碳酸钙得到,所以气体X是 二氧化碳,两次加水发生的都是化合反应,其一是氧化钙和水反应生成氢氧化钙,其二是氧化钙和过氧化氢以及水反应生成CaO2.8H2O,对应的化学方程式依次为CaO+H2O═Ca(OH)2,CaO+H2O2+7H2O═CaO2·8H2O;由于过程中氧化钙遇到了水生成氢氧化钙,所以CaO2·8H2O实际获得的产品不纯,主要含有的固体杂质是 Ca(OH)2;(2)装置A加热的是熟石灰和硫酸铵,生成硫酸钙和氨气以及水,对应的化学方程式 Ca(OH)2+(NH4)2SO4![]() CaSO4+2NH3↑+2H2O;(3)制取CaO2·8H2O的化学方程式为CaCl2 + H2O2+ 2NH3·H2O+ 6H2O=CaO2·8H2O + 2Y。根据质量守恒定律可得,Y的化学式 NH4Cl;该反应一般在0~5℃的低温下进行,由于过程中加入了氨水,氨水是氨气溶解于水形成的溶液,所以温度升高会导致气体溶解度降低而挥发出来,所以温度不能过高的原因是防止NH3·H2O挥发,提高原料利用率;(4)产品性质测定:甲组取产品充分加热,由于信息提示为“加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气”,而检验氧气一般使用带火星的木条,所以可用带火星的木条检验产生的气体。乙组取产品加水,根据信息提示“过氧化钙与水反应生成氢氧化钙和氧气”,生成物为碱性的氢氧化钙,所以滴入无色酚酞溶液,酚酞变红。由于甲组加热后生成了氧化钙,而氧化钙遇到无色酚酞溶液,能和水反应得到碱性的氢氧化钙,使酚酞变红,所以若需得到同样的结论,甲组能采用与乙组相同的方法;(5)由图可以看出失去的结晶水的质量为2.76g-1.32g=1.44g;
CaSO4+2NH3↑+2H2O;(3)制取CaO2·8H2O的化学方程式为CaCl2 + H2O2+ 2NH3·H2O+ 6H2O=CaO2·8H2O + 2Y。根据质量守恒定律可得,Y的化学式 NH4Cl;该反应一般在0~5℃的低温下进行,由于过程中加入了氨水,氨水是氨气溶解于水形成的溶液,所以温度升高会导致气体溶解度降低而挥发出来,所以温度不能过高的原因是防止NH3·H2O挥发,提高原料利用率;(4)产品性质测定:甲组取产品充分加热,由于信息提示为“加热至350℃左右,过氧化钙迅速分解,生成氧化钙,并放出氧气”,而检验氧气一般使用带火星的木条,所以可用带火星的木条检验产生的气体。乙组取产品加水,根据信息提示“过氧化钙与水反应生成氢氧化钙和氧气”,生成物为碱性的氢氧化钙,所以滴入无色酚酞溶液,酚酞变红。由于甲组加热后生成了氧化钙,而氧化钙遇到无色酚酞溶液,能和水反应得到碱性的氢氧化钙,使酚酞变红,所以若需得到同样的结论,甲组能采用与乙组相同的方法;(5)由图可以看出失去的结晶水的质量为2.76g-1.32g=1.44g;
设样品中CaO28H2O的质量为x
CaO28H2O![]() CaO2+8H2O
CaO2+8H2O
216 144
x 1.44g![]()
x=2.16g
样品中CaO28H2O的质量分数为![]() ×100%≈78.3%
×100%≈78.3%
答:①CaO28H2O样品中结晶水的质量=1.44g;②该样品中CaO28H2O的质量分数 78.3%;(6)A、由于甲组实验中生成二氧化碳气体,之后的反应中没有二氧化碳的参与,所以甲组反应的原子利用率不是100%,错误;B、在原料充分转化的前提下,由于甲组中生成了氢氧化钙等杂质,所以甲组的CaO28H2O沉淀过滤后需要洗涤,错误;C、乙组产生的副产品氯化氢由于会和产品反应,所以可能会影响CaO2的产率,正确。故选C。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】酒精灯是实验室中常用的加热仪器,某兴趣小组同学对酒精灯内焰进行如下探究。
(Ⅰ)定性研究
甲同学取一根火柴梗,拿住一端迅速平放入酒精灯火焰中,1~2s后取出,观察到位于焰心的部分没有明显变化,说明焰心温度最低。
(1)写出碳完全燃烧的反应方程式______________________________。
(Ⅱ)定量研究
乙同学用注射器抽取灯芯和焰心交界处气体,利用氧气传感器测量氧气的体积分数(见下表),丙同学利用高温传感器测定酒精灯灯芯和焰心交界处温度(见下表)。
测量次数 | 第一次 | 第二次 | 第三次 |
灯芯和焰心交界处氧气体积分数 | 5.93% | 5.29% | 6.53% |
灯芯和焰心交界处温度/℃ | 236 | 243 | 240 |
(2)乙、丙同学多次进行测量的目的是_____。
(3)火柴梗燃烧需要氧气的最低含量是14.0%,着火点是270℃,结合上表谈谈你对“火柴梗在焰心处没有明显变化”的认识__________________________________。
(4)如果考虑抽气时空气的影响,则乙同学测出的氧气浓度比焰心的实际氧气浓度______。(填“高”或“低”):另外乙同学所测氧气的体积分数差异的原因可能是①_____________________;②__________________________________。