题目内容
【题目】一中“大豪阳”项目学习小组进行了如下探究。
[查阅资料]
①溶液中离子浓度越大,导电性越强,电导率越大。氯化钙溶于水后形成自由移动的CI-和Ca2+。
②鸡蛋壳主要成分是CaCO3,其他成分对实验影响忽略不计。
③鸡蛋壳与牙齿和含氟牙膏反应的化学原理相似。
[实验一]鸡蛋沉浮。
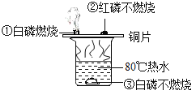
将一个新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
(1)检验上述反应产生的气泡成分的方法为__________________(用化学方程式表示)。
[实验二]鸡蛋壳溶解。
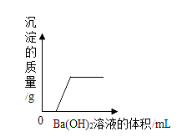
在烧杯中加入稀盐酸,插入电导率传感器,加入蛋壳粉,搅拌,测得电导率随时间的变化如图。
(2)搅拌的目的是________________。
(3)图1中,a-b段电导率变化的原因_______________。
[实验三]鸡蛋壳代替牙齿探究含氟牙膏能否预防龋齿。
查资料知,含氟牙膏(含氟成分为NaF)与蛋壳反应在表面生成氟化钙保护层。反应的化学方程式为:![]()
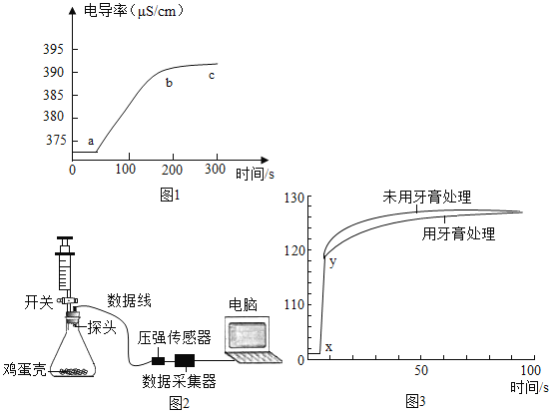
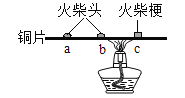
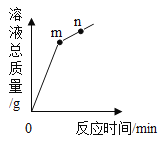
(4)先检查图2装置气密性,方法是________________,再称取0.50g “牙膏处理过的蛋壳(用牙膏液浸泡、洗涤、晾干)”于锥形瓶中,用注射器抽取20mL3.5%的盐酸(模拟形成龋齿的酸境),连接好装置,接下来的操作是_______________,测得压强随时间的变化如图3所示。用“未用牙膏处理的蛋壳”重复上述实验。
(5)图3中x-y段压强增大的主要原因_________________。用“未用牙膏处理的蛋壳”重复上述实验的作用是___________________。
(6)根据实验三的数据分析,含氟牙膏___ (填“ 能”或“不能”)预防龋齿,理由__________________________。
【答案】Ca(OH)2+CO2=CaCO3↓+H2O 增大接触面积,加快反应速率 蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强 打开开关,拉动(或“推动”也可)注射器活塞,松开后,活塞回到原位,说明气密性良好 打开开关,将盐酸快速压入锥形瓶,关闭开关 碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大 对比 能 相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应能产生的气体更少,压强更小,消耗的鸡蛋壳更少
【解析】
(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(2)搅拌是为了增大接触面积,加快反应速率;
(3)图1中,a-b段电导率变化的原因:蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强;
(4)检验装置气密性利用装置内外的压强差检验,所以检查图2装置气密性,方法:打开开关,拉动注射器活塞,松开后,活塞回到原位,说明气密性良好,连接好装置,接下来的操作是:打开开关,将盐酸快速压入锥形瓶,关闭开关,测得压强随时间的变化如图3所 示;
(5)碳酸盐和酸反应会生成二氧化碳,所以对比图3中x-y段压强增大的主要原因:碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大;用“未用牙膏处理的蛋壳”重复上述实验的作用是对比;
(6)根据图3的数据分析,含氟牙膏能预防龋齿,这是因为单位时间内用牙膏处理过的蛋壳产生二氧化碳较少。
故答案为:(1)Ca(OH)2+CO2=CaCO3↓+H2O;
(2)增大接触面积,加快溶解速率;
(3)蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强;
(4)打开开关,拉动(或“推动”也可)注射器活塞,松开后,活塞回到原位,说明气密性良好;打开开关,将盐酸快速压入锥形瓶,关闭开关;
(5)碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大;对比;
(6)能;相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应能产生的气体更少,压强更小,消耗的鸡蛋壳更少。

 阅读快车系列答案
阅读快车系列答案【题目】某小组在探究铜、铁、银三种金属活动性顺序时,从下列药品中选择三种药品进行探究:铜丝、铁丝、银丝、硫酸亚铁溶液、硫酸铜溶液、硝酸银溶液。
请你帮助他们设计并完成两种实验方案:
方案 | 实验药品 | 实验操作 | 实验现象 | 反应方程 | 实验结论 |
方案一 | 铁丝、银丝、硫酸铜溶液 | 把铁丝银丝分别插入到硫酸铜溶液中 | (3)_____ 银丝表面无现象 | 方程式略 | 铁>铜>银 |
方案二 | (1)_____ | (2)_____ | 现象略去 | (4)____ |
【题目】明矾(化学式为KAl(SO4)2·12H2O)是农村常用的一种净水剂,为了探究明矾中每种粒子是否有净水作用,探究小组设计了如下探究环节:
(1)提出问题:明矾在溶液中能全部离解成自由移动的钾离子、铝离子和硫酸根离子,明矾的净水原理是什么?是什么起作用?
(2)猜想与假设:明矾溶于水生成的胶状物与铝离子有关,即明矾净水是铝离子的作用。
(3)探究实验:设计实验、实验过程、分析与论证:
实验步骤 | 实验现象 | 结论 |
①在蒸馏水中加入少量明矾,搅拌 | 明矾溶解 | 明矾能溶解 |
②在浑浊的天然水中加少量明矾,搅拌静置 | 有沉淀生成,天然水变澄清 | 明矾吸附水中小颗粒泥尘聚集而沉降 |
③在浑浊的天然水中加少量硫酸铝,搅拌静置 | 有沉淀生成,天然水变澄清 | 硫酸铝________(是否)具有明矾的吸附作用 |
④在浑浊的天然水中加少量硫酸钾,搅拌静置 | 天然水仍然浑浊 | 硫酸钾____(是否)具有明矾的吸附作用 |
⑤在浑浊的天然水中加少量氯化铝,静置沉淀 | 有沉淀生成,天然水变澄清 | 氯化铝___(是否)具有明矾的吸附作用 |
(4)归纳结论:通过以上五组对比实验可知明矾的净水作用与______有关。