题目内容
【题目】结合下列实验常用装置,回答有关问题.
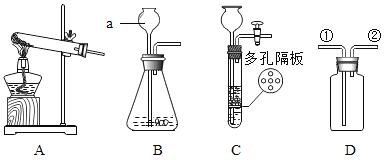
(1)写出图中标有字母的仪器名称a______
(2)实验室用高锰酸钾制取氧气应选择的发生装置是____(填序号),若用D装置用排水法收集氧气,瓶内预先装满水,氧气从____(填①或②)管通入。
(3)实验室常用装置C代替装置B制取气体,装置C的优点是_____,下列反应适用于该装置,体现上述优点的是____(填序号)。
a 碳酸钠粉末和稀硫酸 b 大理石和稀盐酸
c 块状的电石与水常温下反应制乙炔气体 d 过氧化氢溶液与二氧化锰粉末
(4)实验室制取二氧化碳的化学方程式_____。若要制得干燥的二氧化碳气体可在装置D中盛放适量的_____(填物质名称),并将气体从____(填①或②)导管口通入。
【答案】长颈漏斗 A ② 可控制反应的发生与停止 b、c 2HCl+Ca(OH)2=CaCl2+CO2↑+H2O 浓硫酸 ①
【解析】
(1)仪器a为长颈漏斗;
(2)高锰酸钾制取氧气需要的反应装置为固-固加热型,即选用A;若用E装置装满水去收集氧气,因为氧气密度小于水,所以氧气应从②口进入;
(3)C装置加了多孔隔板和止水夹,关闭止水夹,可利用生成气体可使固液分离,达到控制反应发生与停止的目的,所以C的优点在于可控制反应的进行;要体现这个优点,一定是固-液反应,并且固体直径应不小于多孔隔板直径,即固体不为粉末状,所以只有b、c符合;
(4)实验室用大理石和稀盐酸制取二氧化碳,方程式为2HCl+Ca(OH)2=CaCl2+CO2↑+H2O;要制取干燥的二氧化碳气体,则D应盛放浓硫酸,此时气体是流经D装置,不是收集,所以从①进。

【题目】某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
(提出问题)这种淡黄色粉末是什么?有什么性质和用途?
(查阅资料)①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
(猜想与探究)猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
(实验与结论)
实验操作 | 实验现象 | 实验结论 | |
猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 |
| 猜想a、c不成立,猜想b成立。 |
探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有___________ |
②往①试管内的溶液中滴加___________ |
| 生成物有氢氧化钠 |
(继续探究)小组的同学对过氧化钠能作为供氧剂也很感兴趣,大家讨论认为可能是CO2在常温下能与过氧化钠反应有关,于是设计右图所示的装置继续实验探究。
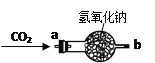
实验操作 | 实验现象 | 实验结论 |
①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: |
②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 |
(交流与比较)与我们学过的制氧气方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是(从两个不同角度回答):________________________________、________________________________。
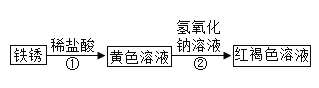
【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.
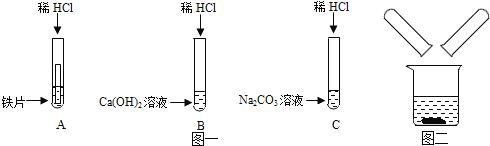
(1)写出A试管中的反应现象_____.
(2)写出B试管中反应的化学方程式_____.
(3)实验结束后,小组同学将_____两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
(提出猜想)
甲同学猜想:NaCl; 乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl; 你的猜想:_____.
(交流讨论)
你认为_____同学的猜想一定不正确,理由是_____.
(设计实验)请设计实验证明你的猜想正确.
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加_____ | _____ | 猜想成立 |
【题目】金属在生产和生活中应用广泛。请回答下列问题。
(1)生活中常用铁锅做饭,主要利用了铁的_____性。
(2)厨房中铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法_____。
(3)铝合金制造的飞机外壳,具有轻量化、能抗击强大气流的冲击、耐受水雾和雨雪侵蚀等特点。这是利用了铝合金的_____、_____等优点(写出两条即可)。
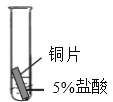
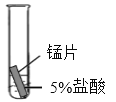
(4)某研究小组为探究铁、铜、锰(Mn)的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用 5%的盐酸体积相同)。
(实验记录与分析)
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | 立即产生气泡,速率较慢 | 无明显现象 | 立即产生气泡,速率较快 |
实验结论 | 铁、铜、锰的金属活动性顺序由强到弱为______>______>_____ | ||
写出实验一试管中铁和盐酸发生反应的化学方程式_________________________________________________________________。