题目内容
【题目】金属及合金是应用广泛的材料。

(1)清洁铝制水壶(如图1)表面时,一般不用钢丝球擦洗,原因是____________。
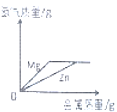
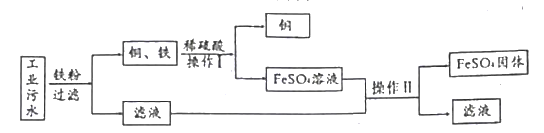
(2)已知,纯铁在1538℃时熔化;生铁是铁的合金;图2是生铁炼钢的过程示意图。
①预测生铁的熔点可能是_____________(填字母编号)
A.1620℃ B.1538℃ C.1250℃
②向生铁熔化形成的生铁水(液态生铁)中加入炼钢料和吹入氧气后,生铁水即转变为钢水。钢水中的含碳量比生铁水____________(填“高”或“低”);不能用空气代替氧气炼钢,因为空气中的氮气从钢水申排出来时会____________而造成钢水在炼钢炉内发生凝固。
【答案】破坏铝表面的氧化膜,使铝受到氧化而被腐蚀 C 低 吸收热量
【解析】
(1)铝金属活动性较强,易与氧化,但其表面生成物--致密的氧化铝薄膜能阻止内部的铝继续被氧化,因此,铝具有很好的抗腐蚀性能,如用钢丝球擦洗铝锅,就破坏了这层保护膜,所以铝锅不宜用钢丝球擦洗的原因是:破坏铝表面的氧化膜,使铝受到氧化而被腐蚀;
(2)①生铁是合金,属于混合物,则生铁的熔点比铁的熔点低,则生铁的熔点应该低于1538℃,故选C;
②根据铁中含有的碳的质量分数的大小,把铁的合金分为生铁和钢;含碳量在2%~4.3%之间的属于生铁,含碳量在0.03%~2%之间的属于钢。钢水中的含碳量比生铁水中的低;
炼钢中选用氧气而不选空气是为了促使反应更加剧烈,并获得更多的热量,维持其他反应进行;不能用空气代替氧气炼钢,因为空气中的氮气从钢水中排出来时会吸收热量而造成钢水在炼钢炉内发生凝固。

【题目】请参与下列实验探究:
(实验探究)
实验内容 | 记录数据 |
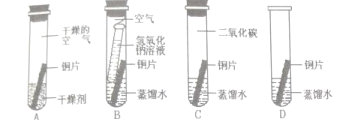
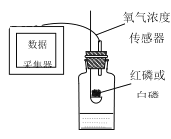
A.借助新型传感设备探究红磷、白磷在空 气中燃烧时的耗氧情况
| 燃烧红磷:瓶内剩余气体的体积分数为8.85% 燃烧白磷:瓶内剩余氧气的体积分数为3.21% |
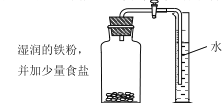
B.用铁生锈原理测定空气中氧气的体积分数
| 反应前测定:广口瓶容积(扣除药品、导管和瓶塞所占容积)为125.0mL 反应后测定:进入广口瓶中的体积为25.0mL |
(1)红磷和白磷是由相同的磷元素组成的不同___________(填“化合物”或“单质”)。进行A实验时,燃烧反应的化学方程式可表示为___________。
(2)实验A的测定结果是在操作无误、装置不漏气,红磷、白磷耗氧差异较大的主要原因___________。
(3)实验B中,下列属于为加快实验进程而采取的措施是___________和___________(填数字编号)。
①在集气瓶中进行 ②塞紧瓶塞不漏气 ③使用铁粉而不使用铁丝 ④加少量食盐
(4)铁生锈的实质是铁与_________(写化学式)发生了化学反应。根据表中记录数据,可计算出空气中氧气的体积分数为__________。
(反思与拓展)
铜在潮湿的空气中生成铜绿化学式为[Cu2(OH)2CO3]时也能耗氧,从化学式可以看出,铜绿的生成是铜与水及空气中的___________发生反应的而过程,所以,实验B_____ (填 “能”或“不能”)用铜粉代替铁粉。
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(学生板演)该反应的化学方程式 .
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
(假设猜想)针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 .
(实验探究)(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 .
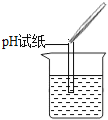
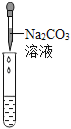
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的.
(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(实验探究)(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是 .
(2)实验方案中也有一个是错误的,错误的原因是 .