题目内容
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(学生板演)该反应的化学方程式 .
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
(假设猜想)针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 .
(实验探究)(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 .
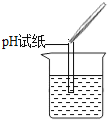
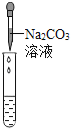
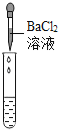
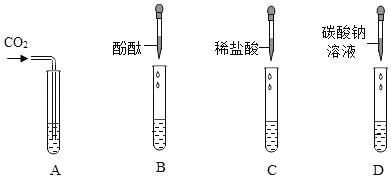
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的.
(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(实验探究)(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
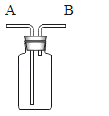
(1)实验操作中的错误是 .
(2)实验方案中也有一个是错误的,错误的原因是 .
【答案】H2SO4+2NaOH═Na2SO4 +2H2O;
猜想四或四;
NaOH或氢氧化钠;
有气泡产生;
pH试纸浸入溶液中;
BaC12与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在(其他合理答案均可)
【解析】
试题【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,注意化学式的写法和配平;
【假设猜想】根据酸碱不能共存判断不合理的猜想;
【实验探究】根据碳酸钠和硫酸反应能生成二氧化碳气体解答;
【评价反思】(1)根据图示操作判断,检测溶液的pH时,pH试纸不能伸入溶液中;
(2)检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀.
解:【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,化学方程式为H2SO4+2NaOH═Na2SO4+2H2O;
【假设猜想】硫酸和氢氧化钠反应生成硫酸钠和水,酸或碱可能过量,但不能同时过量,因为酸碱不能共存,会继续反应,故猜想四不合理;
【实验探究】(1)硫酸铜和氢氧化钠反应能生成氢氧化铜蓝色沉淀,因此溶液中滴加几滴CuSO4溶液,无明显变化,说明溶液中一定没有氢氧化钠.
(2)溶液中有硫酸,滴加碳酸钠后,碳酸钠会和硫酸反应生成二氧化碳气体,因此会看到产生气泡.
【评价反思】(1)根据图示操作判断,检测溶液的pH时,pH试纸不能伸入溶液中,应用玻璃棒蘸取少量溶液涂到pH试纸上;
(2)检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀,故不能证明溶液中一定存在硫酸;
故答案为:【学生板演】H2SO4+2NaOH=Na2SO4+2H2O;
【假设猜想】猜想四;H2SO4和NaOH在溶液中不能共存;
【实验探究】(1)NaOH;(2)有气泡产生;
【评价反思】①pH试纸浸入溶液中;②Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案