��Ŀ����
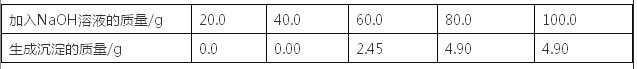
����Ŀ��Ϊ�˽�Լ��ľ��Դ������������ʯͷֽ��ʯͷֽ�����غ�ˮ����ֳ�в����Ĵ������������Ƶã�Ϊ�˲ⶨij�ֱ�����̼��Ƶ�����������ȡ����15��������150��7.3%��������Һ����ַ�Ӧ�Ƶ�ʣ�����ʵ�������Ϊ159.72���������豴�����������ʲ������ᷴӦ��������Ϊ����������ʵ�����ݣ��ɰ����·������㣺���ݡ�150��7.3%��������Һ�����ó��μӷ�Ӧ���Ȼ���������Ȼ����ݷ�Ӧԭ�����̼��Ƶ�������������������̼��Ƶ�����������
��1�����Ϸ����Ƿ���ȷ�� ��
��2�����㱴����̼��Ƶ���������
���𰸡�(1)����ȷ��150��7.3%��������Һ�е��Ȼ���δ��ȫ��Ӧ (2)80%
��������
���������(1)����ȷ���ɷ�Ӧ�Ļ�ѧ����ʽCaCO3+2HCl�TCaCl2+H2O+CO2��̼������Ȼ����������Ϊ100��73����150��7.3%��������Һ����15g̼�����ȫ��Ӧ�����ԣ��Ȼ�����ʣ��ܸ����Ȼ����������㣮�����Ϸ�������ȷ
��2����Ӧ���������غ㶨�ɣ���ѧ��Ӧǰ�����ʵ��������䣬���жϷ�Ӧ������CO2������Ϊ��15g+150g��159.72g=5.28g���ٸ��ݻ�ѧ����ʽ��CaCO3+2HCl�TCaCl2+H2O+CO2����CO2��CaCO3��������ϵ���ɼ����CaCO3����������һ�������������̼��Ƶ���������
�⣺����Ʒ�д���CaCO3������Ϊx
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
x 5.28g
![]() ��ã�x=12g
��ã�x=12g
������̼��Ƶ���������Ϊ��![]() ��100%=80%
��100%=80%
�ʴ�Ϊ����1������ȷ��150��7.3%��������Һ�е��Ȼ���δ��ȫ��Ӧ����2��������̼��Ƶ���������Ϊ80%��

����Ŀ��ͬѧ�Dz������ϣ�þ��һ�ֻ�ѧ���ʷdz����õĽ����������ڶ���������ȼ�ա�ͬѧ������ͼ��ʾװ�÷ֱ����þ���ڶ�����̼�͵�����ȼ�յ�ʵ�顣B�й۲쵽þð������ɫ���̣����ŵ��̼�����ζ��ͬѧ�Ƕ�������Ӧ������̽����
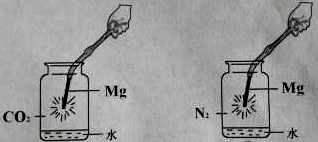
A B
[��������]
������þ��̼��þ�����Ժ����ᷴӦ��
������þ��Mg3N2��������ɫ���壬��ζ����ˮ������ɫ����������þ���������д̼�
����ζ�İ�����NH3����
ʵ��1̽��A�����ɺ�ɫ����Ͱ��̵ijɷ֡�
[���������]1����ɫ������̿��
2�����̿�����MgO ��MgCO3��
[����ʵ��]
ʵ����� | ʵ������ | ʵ����� |
��ȡA�����ɵĹ������Թ��У���������ϡ���� | ��ɫ������ʧ�����������ɡ� | �� |
��������Ӧ���ʣ������ˣ�������ϴ�Ӹ������ʢ�������ļ���ƿ�е�ȼ��Ϩ�����ƿ�е������ʯ��ˮ | ��ɫ����ȼ�գ����⣬���ȣ�����ʯ��ˮ����ǡ� | ��ɫ������̿�� д����ʵ���г���ʯ��ˮ������Ӧ�Ļ�ѧ����ʽ �� |
ʵ��2 ̽��B���ŵ��̼�����ζ��ԭ��
ͬѧ�Ǹ��ݲ��ĵ����Ϸ�����þ���ڵ�����ȼ���ŵ��̼�����ζ��ԭ���뼯��ƿ�е�ˮ�йء�����������ʵ��Ļ����ϣ����һ��ʵ�鷽��֤��ͬѧ�ǵIJ�����ȷ��
��
[��˼������]
ͨ��̽����ͬѧ�Ƕ�ȼ�պ���������µ���ʶ ��
��ʵ��Ӧ�ö���������