题目内容
【题目】人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使叮咬处又痛又痒.化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究.
[提出问题]蚁酸的成分是什么?它有什么性质?
[查阅资料]Ⅰ.蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;
Ⅱ.蚁酸在隔绝空气并加热的条件下会分解生成两种氧化物.
[实验探究]
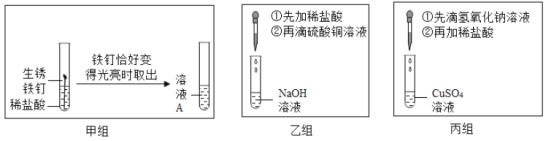
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成_____色,说明蚁酸溶液显酸性;
(2)小芳同学根据蚁酸中含有______元素,推测出一种生成物是水;
(3)另一种生成的氧化物是气体,小敏提出两种猜想:
①猜想Ⅰ:该气体是CO2;猜想Ⅱ:该气体是_____;
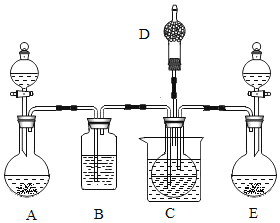
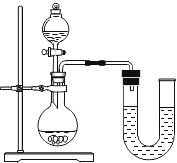
他们将蚁酸分解产生的气体通过如图的装置.
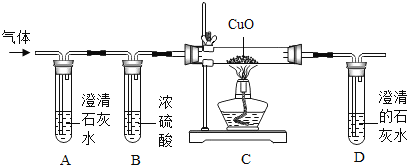
②实验时装置A中无明显变化,则猜想____不成立;若猜想Ⅱ成立,则:
③实验时装置B的作用是_______;
④实验时装置C中的现象是________;
⑤实验时装置D中发生反应的化学方程式为_______;
[讨论交流]从环保角度看,该装置存在明显的缺陷,处理方法是_________;
[拓展延伸]当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒.下列物质中,你不会选择的物质是______
A苏打水 B肥皂水 C食醋 D氨水
【答案】红 H、O CO Ⅰ 干燥CO气体 黑色粉末逐渐变红 CO2+Ca(OH)2=CaCO3↓+H2O 在尾部(b处)放一个燃着的酒精灯 C
【解析】
[实验探究](1)根据酸溶液能使石蕊试液变红色分析;
(2)根据水的组成分析蚁酸中含有的元素;
(3)①根据蚁酸的组成元素分析生成气体;②二氧化碳能使澄清的石灰水变浑浊,据此分析判断;③根据浓硫酸具有吸水性分析装置B的作用;④根据在加热的条件下一氧化碳与氧化铜反应生成了二氧化碳和铜,分析实验时装置C中的现象;⑤根据二氧化碳与氢氧化钙的反应写出反应的方程式;
[讨论交流]根据一氧化碳有毒能污染空气分析处理尾气的方法;
[拓展延伸]根据酸的性质分析选择的物质。
[实验探究](1)蚁酸呈酸性,能使紫色石蕊试液变为红色。故填:红。
(2)根据题意可知,蚁酸在隔绝空气并加热的条件下会分解生成两种氧化物,而蚁酸的化学式为HCOOH,含有氢、氧元素,推测出生成物中有水,故填:H、O。
(3)①由于蚁酸中含有碳、氢、氧三种元素,蚁酸在隔绝空气并加热的条件下会分解生成两种氧化物,一种生成物是水,另一种生成的氧化物是气体,所以,小敏提出的猜想Ⅱ:该气体是CO;②由于二氧化碳能使澄清的石灰水变浑浊,实验时装置A中无明显变化,证明不是二氧化碳气体,则猜想Ⅰ不成立,若猜想Ⅱ成立,则:③由于浓硫酸具有吸水性,实验时装置B的作用是:干燥CO气体;④在加热的条件下一氧化碳与氧化铜反应生成了二氧化碳和铜,实验时装置C中的现象是:黑色粉末逐渐变红;⑤实验时装置D中发生反应是二氧化碳与氢氧化钙发生了反应,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;故填:CO;I;干燥CO气体;黑色粉末逐渐变红;CO2+Ca(OH)2═CaCO3↓+H2O。
[讨论交流]由于一氧化碳有毒能污染空气,从环保角度看,该装置存在明显的缺陷是缺少尾气处理,处理方法是:在尾部(b处)放一个燃着的酒精灯;故填:在尾部(b处)放一个燃着的酒精灯。
[拓展延伸]由于蚁酸是一种酸,能与苏打水、肥皂水、氨水反应,在叮咬处涂抹上述物质可减轻痛痒,不能与食醋反应,不能选择食醋,故选:C。