题目内容
【题目】“84”消毒液具有漂白、杀菌、消毒功效。新冠肺炎疫情发生以来,人们常用“84”消毒液对室内外进行消毒杀菌。某化学兴趣小组对一瓶敞口久置的“84”消毒液成分产生兴趣,于是在老师的指导下,展开探究。
(提出问题)该敞口久置的消毒液中溶质有哪些?
(查阅资料)①“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠(NaCl),NaClO为有效成分,具有腐蚀性并易与空气中CO2反应,(2NaClO+CO2+H2O═2HClO+Na2CO3)。②NaClO溶液、HClO都能使有色布条褪色,具有漂泊、杀菌、消毒功效,HClO特别不稳定,受热或光照会发生分解生成氯化氢和氧气,从而失去其功效。
(分析讨论)小组同学经过讨论,认为敞放的“84”消毒液中的溶质一定有_____,可能还有NaClO、Na2CO3、HClO中的一种或多种。
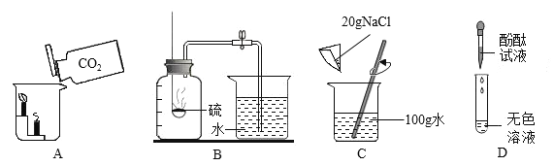
(实验过程)Ⅰ:向装入有色布条的试管中加入适量该消毒液试样,布条长时间不退色。
Ⅱ:另取适量该消毒液试样于试管中,加入足量氯化钙溶液,静置,观察到的现象为_______。
(得出结论)实验过程Ⅰ中有色布条不褪色,说明该消毒液试样中的溶质不含_____,实验过程Ⅱ中反应的化学方程式为 __________ 。 综上所述,该消毒液试样中的溶质为_______ 。
(交流反思)生活中,“84”消毒液贮藏时应注意______;根据题干中所描述的“84”消毒液的性质,___(填“能用”或“不能用”)“84”消毒液对蔬菜和水果进行消毒。
【答案】NaCl 有白色沉淀生成 NaClO、HClO Na2CO3+CaCl2=CaCO3↓+2NaCl NaCl 、Na2CO3 密封、避光保存 不能用
【解析】
分析讨论:
因为“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,氯化钠的化学性质稳定,所以该消毒液中的溶质一定有NaCl;
实验过程:
Ⅰ:向装入有色布条的试管中加入适量该消毒液试样,布条长时间不退色,说明该消毒液试样中不含具有氧化性的物质:NaClO、HClO,因此NaClO全部转化为碳酸钠。
Ⅱ:另取适量该消毒液试样于试管中,由Ⅰ知消毒液中含碳酸钠,加入足量氯化钙溶液,碳酸钠与氯化钙反应生成氯化钠和碳酸钙白色沉淀,静置,观察到的现象为有白色沉淀生成。
得出结论:
实验过程Ⅰ中有色布条不褪色,说明该消毒液试样中不含具有氧化性的物质:NaClO、HClO;
碳酸钠与氯化钙反应生成氯化钠和碳酸钙白色沉淀,反应的化学方程式为:![]() ;
;
由以上实验现象分析可知,该消毒液试样中的溶质为NaCl 、Na2CO3;
交流反思:
因为NaClO有腐蚀性并易与空气中二氧化碳反应,HClO不稳定,受热或光照会发生分解,所以84消毒液应密封、避光保存;“84”消毒液具有漂白性,所以不能用“84”消毒液对蔬菜、水果进行消毒。

【题目】阅读下面材料,回答问题。
硫元素广泛存在于自然界中,在火山口附近有硫单质存在,地球表面的含硫化合物主要以矿物质形式存在,如石膏(CaSO42H2O)、芒硝(Na2SO410H2O)等。硫单质是一种淡黄色的固体,不溶于水,易溶于二硫化碳(CS2)。火山喷发时,部分硫元素转化成硫化氢气体;部分硫元素转化成二氧化硫和三氧化硫气体,二氧化硫在大气中易被氧化成三氧化硫,二氧化硫和三氧化硫溶于水,分别生成亚硫酸和硫酸。
(1)从物质类别和硫元素化合价角度,对硫及其化合物进行分类,根据表中物质组成规律,补充缺项。
物质类别 | 单质 | 氢化物 | 氧化物 | 酸 | 盐 |
化学式 | S | H2S | SO2 | H2SO3 | _____ |
SO3 | H2SO4 | Na2SO4 |
(2)结合材料中硫单质的性质分析,如果洗去粘在试管壁上的硫,应选用的试剂是____。
(3)硫化氢中硫元素的化合价为________;硫化氢的水溶液称为氢硫酸,氢硫酸露置在空气中与氧气发生置换反应,产生淡黄色沉淀,写出化学方程式_________;氢硫酸敞口放置在空气中,溶液的pH__(填“增大”“减小”或“不变”)。
(4)从物质类别的角度预测,下列物质与二氧化硫、三氧化硫均能发生化学反应的是_______(填序号)。
a O2 b NaOH c H2O d HCl
(5)H2SO3不稳定,易分解产生气体(与H2CO3类似)。写出稀硫酸与亚硫酸钠(Na2SO3)溶液发生复分解反应的化学方程式________。
【题目】KCl和KNO3在不同温度下的溶解度数据如表所示,下列说法中正确的是
温度/℃ | 20 | 30 | 60 | |
溶解度/g | KCl | 33 | 38 | 45 |
KNO3 | 31 | 64 | 110 |
A. 60℃时,100g水中最多溶解45 g KCl
B. 随着温度的升高,某饱和KCl溶液中会有固体析出
C. KNO3的溶解度始终大于KCl
D. 60℃时,某KNO3溶液中溶质的质量分数一定为 ![]()