题目内容
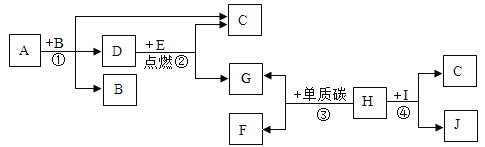
【题目】某化学兴趣小组开展的氢氧化钠性质系列探究活动如下图所示。
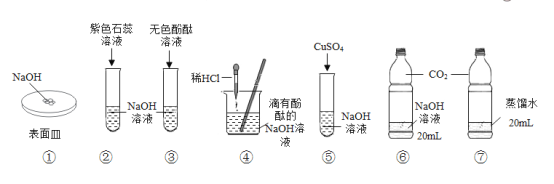 回答下列问题:
回答下列问题:
(1)实验①观察到氢氧化钠表面变______。
(2)实验②观察到紫色石蕊溶液变成______色,实验③观察到无色酚酞溶液变成____色。由此得出:碱溶液能使指示剂变色。
(3)实验④: I.当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有____(填化学式)。
Ⅱ.如图是氢氧化钠与盐酸反应的微观模拟示意图:
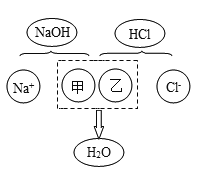
从微观的角度分析,甲、乙两处应填入的离子符号分别为____、______。
(4)实验⑤观察到的现象是_________,说明碱溶液能与某些盐反应。该反应的化学方程式为______。
(5)实验④⑤对应的化学反应,属于中和反应的是____(填数字序号)。
(6)实验⑥⑦为用软矿泉水瓶所做的对比实验,装__的软矿泉水瓶变瘪更明显,原因是______(用化学方程式表示)。
【答案】潮湿 蓝 红 无 NaCl、HCl OH- H+ 产生蓝色沉淀 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 ④ 氢氧化钠溶液 2NaOH + CO2= Na2CO3+ H2O
【解析】
(1)氢氧化钠在空气中易吸收水蒸气而潮解,实验①观察到氢氧化钠表面变潮湿;
(2)氢氧化钠溶液呈碱性,能使紫色的石蕊溶液变蓝色,无色的酚酞变红色。实验②观察到紫色石蕊溶液变成蓝色,实验③观察到无色酚酞溶液变成红色。由此得出:碱溶液能使指示剂变色;
(3)I.氢氧化钠与盐酸反应生成氯化钠和水,氯化钠溶液呈中性,酚酞遇中性溶液呈无色。当滴加稀盐酸至溶液呈中性时,溶液显无色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有氯化钠和氯化氢,化学式分别为:NaCl、HCl;
Ⅱ.氢氧化钠与盐酸的实质是氢氧化钠中氢氧根离子与盐酸中的氢离子结合生成水,从微观的角度分析,甲、乙两处应填入的离子符号分别为OH-、H+;
(4)氢氧化钠与硫酸铜反应生成氢氧化铜和硫酸钠。实验⑤观察到的现象是产生蓝色沉淀,说明碱溶液能与某些盐反应。该反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(5)中和反应是酸与碱反应生成盐和水的反应,实验④是氢氧化钠与盐酸反应生成氯化钠和水,属于中和反应;实验⑤是氢氧化钠与硫酸铜反应生成氢氧化铜和硫酸钠,是碱与盐反应生成另一种碱和另一种盐。实验④⑤对应的化学反应,属于中和反应的是④;
(6)氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钠溶液能吸收二氧化碳气体,使软矿泉水瓶中的气压降低。实验⑥⑦为用软矿泉水瓶所做的对比实验,装氢氧化钠溶液的软矿泉水瓶变瘪更明显,原因是2NaOH + CO2= Na2CO3+ H2O。

 备战中考寒假系列答案
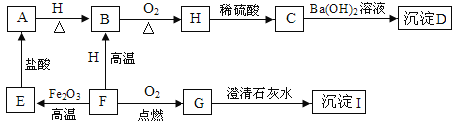
备战中考寒假系列答案【题目】菱镁矿中主要含MgCO3、FeCO3和SiO2。以菱镁矿为原料制取镁的工艺流程如下。
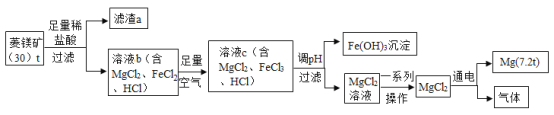
回答下列问题:
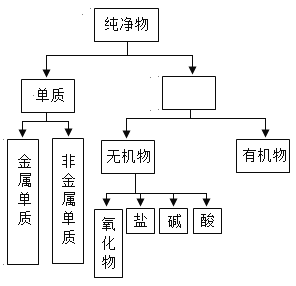
(1)菱镁矿属于___(选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是___。
(3)写出菱镁矿中MgCO3与稀HC1反应的化学方程式___。
(4)溶液b→溶液c反应的化学方程式为:![]() (补充完方程式)____。
(补充完方程式)____。
(5)溶液c调pH使Fe2+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8-__。
已知:物质沉淀的pH见下表:
物质 | Mg(OH)2 | Fe(OH)3 |
开始沉淀的pH | 8.9 | 1.5 |
完全沉淀的pH | 10.9 | 2.8 |
(6)结合流程中的数据计算。
①菱铁矿中镁元素的质量分数为_____(不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量____(写出计算过程)。
【题目】兴趣小组设计实验探究氢氧化钠的性质,请你参与他们的探究。
(实验过程与分析)
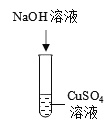
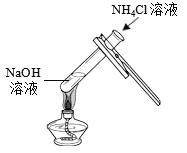
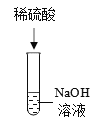
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | __________ | __________ | 无明显现象 |
实验结论 | 氢氧化钠能与硫酸铜发生反应 | 氢氧化钠能与氯化铵发生反应 | 氢氧化钠不能与硫酸发生反应 |
(1)实验一的现象:___________。
(2)实验二的现象:__________。
(实验反思与拓展)
(3)实验一中发生反应的化学方程式: _____。
(4)某同学认为实验三的结论不正确,他改进了该实验方案:先向氢氧化钠溶液中滴入几滴酚酞溶液并振荡,再滴入稀硫酸,观察到溶液由____色变为无色,由此可知氢氧化钠与稀硫酸确实发生了反应,该反应的化学方程式为__________。
(5)由实验三联想到二氧化碳通入到氢氧化钠溶液中也没有明显现象,那么二氧化碳与氢氧化钠是否发生了化学反应呢? (本实验中忽略CO2溶于水)
①甲同学设计了如图所示实验方案,当观察到_________现象时,说明两者发生了化学反应。
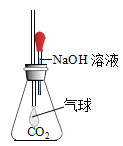
②乙同学重新设计实验方案:取NaOH溶液于试管中,通入少量CO2,然后向所得溶液中加入____溶液,当观察到_____现象时,也能证明二氧化碳与氢氧化钠发生了化学反应。