题目内容
【题目】某化学课堂正在进行,以下是教学片断。请你参与他们的学习并完成相关任务。
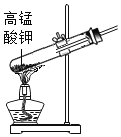
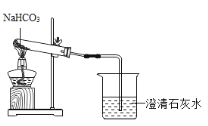
(演示实验)老师按如图所示连接好装置,加入NaHCO3粉末,点燃酒精灯,对试管预热后集中加热,烧杯中澄清石灰水变浑浊,说明生成了CO2.继续加热至无气体产生后撤出导管,熄灭酒精灯。
(问题提出)实验后,同学们对试管中剩余的固体粉末产生了兴趣:剩余粉末由什么物质组成?
(猜想假设)在老师的指导下,同学们对固体粉末作出了如下猜想:
猜想一:NaOH;猜想二:NaOH和Na2CO3;猜想三:Na2CO3。
(实验探究)
实验方案 | 实验操作 | 实验现象 |
方案一 | 取适量粉末溶于水后向溶液中滴入2滴酚酞溶液,摇匀 | 溶液由无色变红色 |
小明根据实验现象认为猜想一成立。小组讨论后,大家认为小明的结论不合理,理由是_____。
实验方案 | 实验操作 | 实验现象 | 实验结论 | |
方案二 | 步骤一 | 取适量粉末溶于水后加 入过量的BaCl2溶液 | _____ | 猜想一不成立 |
步骤二 | 取步骤一的上层清液加入MgCl2溶液2﹣3mL | 无明显现象 | 猜想三成立 | |
(评价交流)小华认为步骤二也可以用MgSO4代替MgCl2,大家不同意他的观点,理由是_____。
(拓展延伸)请你总结上述实验成果,写出碳酸氢钠受热分解的化学方程式_____。
【答案】碳酸钠溶液呈碱性,也能使无色酚酞试液变红色 溶液变浑浊,有白色沉淀生成 MgSO4能和过量的氯化钡反应生成白色沉淀,影响氢氧根离子的检验 2NaHCO3![]() Na2CO3+H2O+CO2
Na2CO3+H2O+CO2
【解析】
[实验探究]
方案一:
碳酸钠溶液呈碱性,也能使无色酚酞试液变红色,所以不能因为溶液能使无色酚酞试液变红色,就认为溶液是氢氧化钠溶液;
方案二:
步骤一:因为方案一不成立,所以溶液中含有碳酸钠,碳酸钠和氯化钡反应生成碳酸钡白色沉淀,故现象为:溶液变浑浊,有白色沉淀生成;
[评价交流]
不能用MgSO4代替MgCl2,因为MgSO4能和过量的氯化钡反应生成白色沉淀,影响氢氧根离子的检验;
[拓展延伸]
根据以上实验可知碳酸氢钠受热反应生成氯化钠、水和二氧化碳,化学方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。
故答案为
[实验探究]
方案一:
碳酸钠溶液呈碱性,也能使无色酚酞试液变红色;
方案二
步骤一:溶液变浑浊,有白色沉淀生成;
[评价交流]
MgSO4能和过量的氯化钡反应生成白色沉淀,影响氢氧根离子的检验
[拓展延伸]
2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。

【题目】图表法是一种常用的数据处理方法,也是化学学习的重要工具。请结合所给图表回答问题。
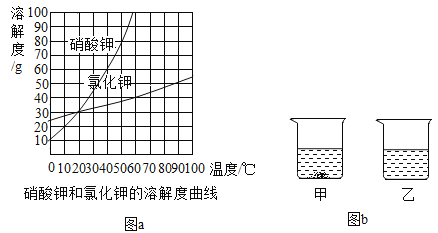
(1)图a是硝酸钾和氯化钾的溶解度曲线。25℃将等质量的氯化钾和硝酸钾分别加入到各盛有 100g 水的两个烧杯中,充分搅拌后得无色溶液,降温至 15℃时 出现如图 b 所示现象。烧杯甲中溶解的溶质是________________________(填化学式)。 硝酸钾中含有少量氯化钾,应采用____________的方法提纯硝酸钾。
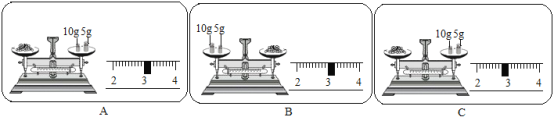
(2)如图数轴中 A、B、C 处表示的是常温时将氯化钠、硝酸铵、烧碱三种物质 分别溶于 100g 水所得溶液的温度,其中表示硝酸铵的是__________填序号)。

(3)如图是氢氧化钠和碳酸钠在不同温度不同溶剂中的溶解度表。
溶质 溶解度 溶剂 | 氢氧化钠 | 碳酸钠 | ||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |
20℃时,若将 0.8g 氢氧化钠分别投5g 酒精的大试管中,振荡,再向 其中通入 CO2,观察到的实验现象为__________________,反应方程式为__________________________。