题目内容
【题目】铜、铁是人类使用最早、应用广泛的金属。
(探究一)
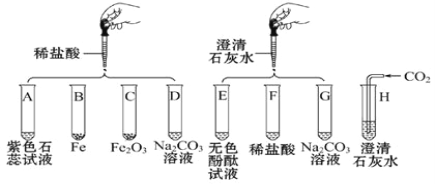
(1)铁生锈主要跟空气中的______有关,用稀硫酸除铁锈的化学方程式为________。
(2)小茜同学发现自己的铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称“铜绿”,主要成分为Cu2(OH)2CO3,该反应的化学方程式为:2Cu+O2+H2O+X = Cu2(OH)2CO3,则X的化学式为__________。
(探究二)
以黄铜矿(CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu。
4CuSO4+2Fe2(SO4)3+2H2O,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu。
(3)CuFeS2为二硫化亚铁铜,也可以表示为CuSFeS,其中S元素的化合价为_____。
(4)发生主要反应的两个化学方程式为:①Fe+Fe2(SO4)3=3FeSO4; ②_________。
(5)FeSO4溶液经蒸发浓缩、_______、过滤等操作得到硫酸亚铁晶体(FeSO4xH2O)。
(探究三)
硫酸亚铁晶体(FeSO4xH2O)是一种重要的食品和饲料添加剂,对其进行热分解研究。
(查阅资料)①硫酸铜粉末为白色,吸水后变成蓝色晶体。
②二氧化硫能使高锰酸钾溶液褪色
③硫酸亚铁晶体加热会先失去结晶水,高温会继续分解产生一种金属氧化物和两种非金属氧化物。
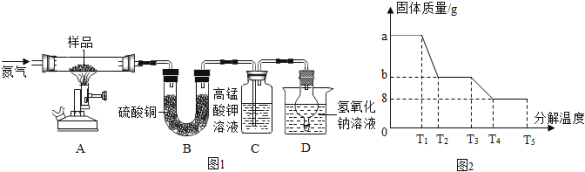
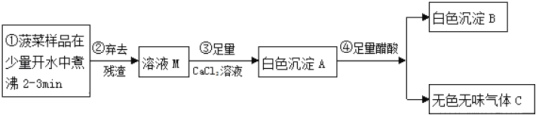
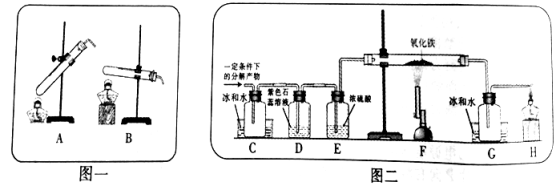
称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出x的值。
(6)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有_______,装置C中高锰酸钾溶液褪色,说明产物中还有_________;装置D球形干燥管的作用_____;实验中要持续通入氮气,否则测出的x会_________(填“偏大”、“偏小”或“不变”)。
(7)硫酸亚铁晶体完全分解后,装置A中残留红棕色固体,另从理论上分析得出硫酸亚铁分解还生成另一物质SO3,写出FeSO4分解的化学方程式_______。
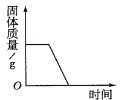
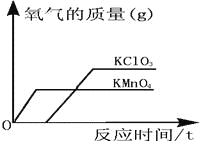
(8)某研究所利用热分析仪对硫酸亚铁晶体(FeSO4xH2O)进行热分解,获得相关数据,绘制成固体质量——分解温度的关系图如图2,根据图2中有关数据,可计算出FeSO4xH2O中的x=______。
【答案】水和氧气 Fe2O3+3H2SO4===Fe2(SO4)3+3H2O CO2 -2 Fe+CuSO4=== CuSO4+Fe 降温结晶(或冷却结晶) 水 二氧化硫 防止氢氧化钠溶液倒吸 偏小 2FeSO4![]() Fe2O3+SO2↑+SO3↑ 7
Fe2O3+SO2↑+SO3↑ 7
【解析】
探究一:
(1)铁和空气中的氧气和水共同接触会生锈;利用稀硫酸除铁锈是稀硫酸和氧化铁反应生成硫酸铁和水,化学方程式为:Fe2O3+3H2SO4===Fe2(SO4)3+3H2O;
(2)根据质量守恒定律,反应前后原子的种类和数目不变,反应前有2个铜原子,三个氧原子和2个氢原子,反应后有2个铜原子、2个氢原子、5个氧原子和1个碳原子,则X中含有2个氧原子和一个碳原子,X为二氧化碳;
探究二:
(3)化合物中各元素的化合价代数和为零,CuFeS2中亚铁元素和铜离子的的化合价为+2价,则(+2)+(+2)+2X=0,得X=-2,即硫元素的化合价是-2价;
(4)根据4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O,生成物是CuSO4、2Fe2(SO4)3,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu,则反应为Fe+Fe2(SO4)3=3FeSO4,和铁和硫酸铜反应生成硫酸铜和铁,方程式为:Fe+CuSO4===CuSO4+Fe;
4CuSO4+2Fe2(SO4)3+2H2O,生成物是CuSO4、2Fe2(SO4)3,向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu,则反应为Fe+Fe2(SO4)3=3FeSO4,和铁和硫酸铜反应生成硫酸铜和铁,方程式为:Fe+CuSO4===CuSO4+Fe;
(5)物质结晶的方法有:浓缩结晶、降温结晶、过滤等;
探究三:
(6)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中还有二氧化硫,装置D球形干燥管的作用防止氢氧化钠溶液倒吸,持续通氮气使得加热产生的水蒸气全部进入U型管中,否则生成的部分水蒸气会在装置A处玻璃管内冷凝,水蒸气停留在装置中导致结果偏小;
(7)根据题中提示,反应物是硫酸亚铁,红棕色固体是氧化铁,生成物还有二氧化硫和三氧化硫,则方程式为:2FeSO4![]() Fe2O3+SO2↑+SO3↑;
Fe2O3+SO2↑+SO3↑;
(8)由图象可知剩余固体为氧化铁质量为8g,而氧化铁中的铁全部来自于硫酸亚铁,又因为FeSO4xH2O中铁原子和水分子的个数比为1:x,则有
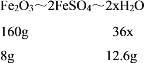
![]()
解得:X=7