题目内容
【题目】水是人类宝贵的自然资源。
(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和__________(填仪器名称)。
(2)在电解水的实验中,与电源正极相连的玻璃管上方产生的是____气。
(3)甲和乙两种固体物质的溶解度曲线如图所示。
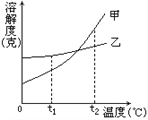
①将t1℃的甲和乙饱和溶液各100g升温至t2℃,此时两种溶液中溶剂的质量:甲____乙(填“>”、“=”或“<”)。
②乙物质中含有少量的甲,可采用__________________法将乙物质提纯。
【答案】 玻璃棒 氧气(O2) > 蒸发结晶
【解析】根据所学知识和题中信息知,(1)用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒。(2)在电解水的实验中,与电源正极相连的玻璃管上方产生的是氧气。(3)甲和乙两种固体物质的溶解度曲线。①甲乙两物质的溶解度均是随温度的升高而增大,t1℃时乙物质的溶解度比甲大,溶解度均是随温度的升高而增大,甲和乙饱和溶液各100g,甲溶液的溶剂比乙多,将t1℃的甲和乙饱和溶液各100g升温至t2℃,此时两种溶液中溶剂的质量:甲>乙。②甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高而变化不大,乙物质中含有少量的甲,可采用蒸发结晶法将乙物质提纯。
点睛∶过滤常用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒。甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高而变化不大,乙物质中含有少量的甲,可采用蒸发结晶法将乙物质提纯。

【题目】小明拿起家中的水壶准备煮水时,发现壶内有些褐色的固体。为了探究其成分,与兴趣小组同学查阅资料后获知这些褐色的固体是水垢,它可能是因为水中含有Ca(HCO3)2和Mg(HCO3)2等可溶性物质在加热时生成了CaCO3和Mg(OH)2。
(1)含有较多Ca(HCO3)2的水称_____(填“硬水”或“软水”),加热时发生反应的化学方程式为__________。
(2)小明认为本市属喀斯特地貌,以石灰岩为主,该水垢的成分只有CaCO3;但小白不同意,认为也可能只有Mg(OH)2,还可能______________。
(3)小明为了证明自己的猜想,设计如下实验方案:
实验操作 | 现 象 | 结 论 |
①取少量水垢于试管中,加入过量的_______。 | 观察到现象_________, 反应的化学方程式__________。 | 水垢中有CaCO3 |
②向①反应后的试管中滴加2-3滴NaOH溶液 | 观察到现象__________。 | 水垢中没有Mg(OH)2, 我的猜想成立 |
(4)小白不认可小明的结论,认为他的实验操作有缺陷,原因是_________________________。