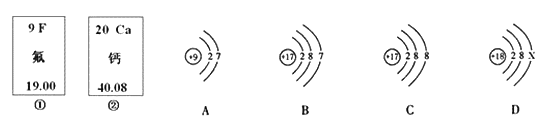
��Ŀ����
����Ŀ�����������ʵ��װ�ã��Ķ��������ϣ��ش����⣺
���ϣ�����(NH3)��������һ�־��д̼�����ζ����ɫ���壬�������нϴ��ԣ��ܶȱȿ���С����������ˮ����ˮ��Һ�Լ��ԡ�ʵ���ҿ��ü����Ȼ��(NH4Cl)����ʯ�����ֹ���ķ�����ȡ������ͬʱ�����Ȼ��ƺ�ˮ�����������ˮ��Ca(OH)2����ˮ��CaCl2��Һ�����ԣ�NH4Cl��Һ�����ԡ�
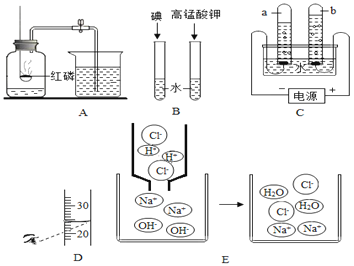
(1)ʵ������ȡ�����Ļ�ѧ����ʽΪ_____��Ӧѡȡ�ķ���װ����_____(��װ�ñ��)��
(2)��Cװ���ռ�����ʱ������Ӧ��_____��ͨ��(����a������b��)�����鰱������ʪ���_____ʯ����ֽ(������ɫ��������ɫ��)��
(3)ijͬѧ�Գ�ַ�Ӧ��Ӧ���ڵĹ�����������һ���о���
��������⣩�������ʵijɷ���ʲô��
���������룩����I��Ca(OH)2��NH4Cl��CaCl2
����II��Ca(OH)2��CaCl2
����III��NH4Cl��CaCl2
����IV��ֻ��CaCl2
��ͬѧ����������������ɣ���һ�ֲ��벻����������Ϊ��_____��
��ʵ��̽������ȡ��Ӧ���������������Թ��У���ˮ�ܽ⡢���ˣ��õ���Һ��
��ȡ������Һ���Թ��У��μ���ɫ��̪��Һ��Һ����ɫ�ޱ仯��˵��_____(��һ�ֲ���)����ȷ��
����ȡ������Һ����һ�Թ��У��μ�AgNO3��Һ��������ɫ��������ͬѧ��Ϊ�����к���NH4Cl�����ǵó����۲���III��ȷ������Ϊ��ͬѧ�Ľ���_____(����������������������)��������_____��
�����۷�˼����ͬѧ��Ϊʵ��װ�����в���֮������������Ľ���ʩ��_____��
���𰸡� 2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3�� B b ��ɫ ����I ����II ������ �Ȼ���Ҳ�ܺ���������Ӧ���ɰ�ɫ���� ��Cװ�õ�a��������β��������װ��
CaCl2+2H2O+2NH3�� B b ��ɫ ����I ����II ������ �Ȼ���Ҳ�ܺ���������Ӧ���ɰ�ɫ���� ��Cװ�õ�a��������β��������װ��
��������
��1��ʵ���ҿ��ü����Ȼ��(NH4Cl)����ʯ�����ֹ��巴Ӧ�����Ȼ��ơ�������ˮ����Ӧ����ʽΪ2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3�����÷�Ӧ�ķ�Ӧ���״̬�ǹ�������Ӧ�����Ǽ��ȣ���ѡ�̹̼�����װ��B��
CaCl2+2H2O+2NH3�����÷�Ӧ�ķ�Ӧ���״̬�ǹ�������Ӧ�����Ǽ��ȣ���ѡ�̹̼�����װ��B��
��2��Cװ���Ƕ��װ�ã���Cװ���ռ�����ʱ�����ڰ����ܶȱȿ���С��ѡ�����ſ������ռ���������Ӧ��b��ͨ�룻���鰱������ʪ��ĺ�ɫʯ����ֽ��������Ϊ�����ܹ�ˮ��Ӧ���ɰ�ˮ����ˮ�Լ��ԣ���ʹʪ��ĺ�ɫʯ����ֽ������
��3���������ƺ��Ȼ�鱗��ܹ������ʲ���1��������ȡ������Һ���Թ��У��μ���ɫ��̪��Һ��Һ����ɫ�ޱ仯��˵����Һ���Լ��ԣ�����Һ�в������������ƣ�˵������II����ȷ����ͬѧ�Ľ��۲��������������Ȼ���Ҳ�ܺ���������Ӧ���ɰ�ɫ����������(NH3)��������һ�־��д̼�����ζ����ɫ���壬�������нϴ��ԣ�����Ҫ��������β����������Ҫ��a���ܴ���װ���հ�����װ�á�

����Ŀ��������ֵ���ijʵ��С���ڿ���������һ��̽��ʵ��:
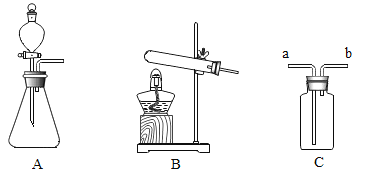
(1)��a�Թ��м���Լ2mL����ͭ��Һ��Ȼ����뼸������������Һ,�۲쵽��������_____��
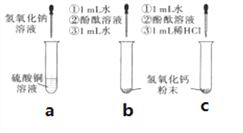
(2)��b��c��֧�Թ��и�����������ͬ�������������Ʒ�ĩ��Ȼ�������1mLˮ,��,�ʻ���״������,�ٸ�����1~2 �η�̪��Һ,�۲쵽���Թ���Һ����졣������b�Թ��м���Լ1mLˮ������c�Թ��м���Լ1mLϡ����,������b�Թܱ��������Һ�Գʺ�ɫ��c�Թܱ����,��Һ�����ɫ����b�Թ��еڶ��μ���Լ1mLˮ��������________��
��������⣩�Թ�c�м���Լ1mLϡ�����,��Һ�е�������ʲô?
����������������������CaCl2��Һ�����ԡ�
��������裩С��������I.CaCl2 ��.CaCl2��HCl ��.CaCl2��Ca(OH)2
����˼���ɣ�С���Բ���������������������___________
������ʵ�飩С��ͬѧͨ������,�������ʵ�鷽��������֤:
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ����c�Թ��е���Һ���Թ���,_______ | ________ | ���������� |
ʵ�����,С��ͬѧ��a��b��c��֧�Թ��е�ʣ�����ʻ��,���ַ�Һ�ʻ��ǡ�
�������뽻������Һ�д������ڵ���������_______��д����Һ�п��ܷ�����Ӧ��һ����ѧ����ʽ________��