题目内容
【题目】同学们从山上采集到一种石灰石,他们取100g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
反应后固体的质量m∕g | 100 | 92 | 84 | 78 | 72 | 67 | 67 |
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为__________g。
(2)求该石灰石中CaCO3的质量分数(即CaCO3在石灰石中所占的百分含量),写出计算过程________。
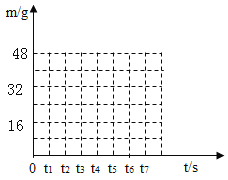
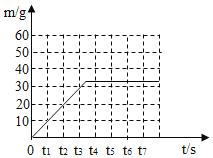
(3)请在如图所示的坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线________。
【答案】33 75%。 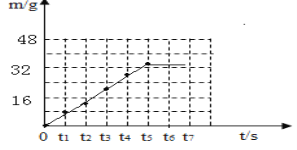
【解析】
首先根据质量守恒定律得出固体质量减小的量即为生成的气体的质量,然后根据气体的质量可以求出样品中碳酸钙的质量.根据表中数据画出图象
解:(1)由于碳酸钙高温分解生成氧化钙和二氧化碳,固体的质量由100g变为67g,减少了33g,说明生成CO2气体的质量为33g;
(2)设样品中含CaCO3的质量为x,则:
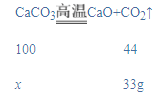
![]()
x=75g,
石灰石中CaCO3的质量分数=![]() ×100%=75%;
×100%=75%;
(3)根据表中数据可知:煅烧时生成气体的质量(m)随时间(t)变化的曲线如图所示:
 。
。

 名校课堂系列答案
名校课堂系列答案【题目】俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于编制出了现代元素周期表的雏形表。下表为元素周期表的部分元素的部分信息,利用下表回答相关问题。
第一周期 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
第二周期 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
第三周期 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)请画出16号元素的原子结构示意图__________,化学反应中该原子比较容易__________电子变成离子;
(2)![]() 表示的是________,其与17号元素形成的化合物是________
表示的是________,其与17号元素形成的化合物是________
(3)同一纵列元素原子的结构特点是________________
(4)上表中第二、三周期元素最外层电子数的变化规律是___________