题目内容
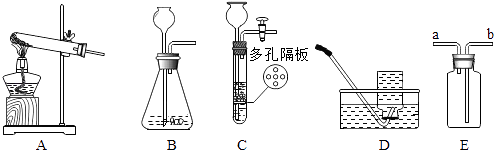
【题目】众所周知,酚酞溶液遇NaOH溶液变红.但是,在分组实验中(如图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物.
【提出问题】分组实验中,出现意想不到的现象的原因是什么呢?
【查阅资料】酚酞溶液由酚酞固体溶于酒精配制而成.
【猜想与假设】
Ⅰ.红色褪去,与NaOH溶液和空气中的CO2反应有关.
Ⅱ.红色褪去,与NaOH溶液的浓度有关.
Ⅲ.出现白色浑浊物,与酚酞溶液的浓度有关.
【进行实验】
实验 | 实验操作 | 实验现象 | |
1 | 向盛有2mL Na2CO3溶液的试管中 | 溶液变红 | |
2 |
| 1号试管0.1min红色褪去 | |
3 | 取3支试管,分别加入2mL水, . | 酚酞溶液浓度/% | 浑浊程度 |
5 | 大量浑浊物 | ||
2 | 少量浑浊物 | ||
0.5 | 无浑浊物 | ||
(1)补充上表中横线处内容:
(2)NaOH与CO2反应的化学方程式为 .
(3)实验1的现象表明,猜想与假设1(填“成立”或“不成立”).
(4)由实验2得出结论:出现“溶液变红后褪色”现象的原因是 .
(5)实验3的操作步骤:取3支试管,分别加入2mL水, .
(6)【反思与评价】依据现有实验,为了确保红色不变,若酚酞溶液浓度为0.5%,建议选用NaOH溶液的浓度为 %.
(7)有同学认为,仅通过实验3得出“猜想与假设Ⅲ成立”证据不足,理由是 .
【答案】
(1)分别向三支试管中滴加5滴5%,2%,0.5%的酚酞溶液
(2)CO2+2NaOH=Na2CO3+H2O
(3)不成立
(4)与NaOH浓度有关,浓度过高会使酚酞褪色
(5)分别向三支试管中滴加5滴5%,2%,0.5%的酚酞溶液
(6)0.5
(7)未排除酒精对酚酞溶解的影响
【解析】解:(1)根据后面的空可知此空位设置变量(2)二氧化碳和氢氧化钠反应产生碳酸钠和水,故反应的方程式为:CO2+2NaOH=Na2CO3+H2O;(3)实验1中碳酸钠和酚酞试液,没有褪色,说明猜想1不成立;故答案为:不成立;(4)表格中的实验2选择的氢氧化钠溶液不同,氢氧化钠的浓度越高,酚酞越容易褪色,故答案为:与NaOH浓度有关,浓度过高会使酚酞褪色;(5)根据实验3的现象可知是选择不同浓度的酚酞试液探究猜想3,故答案为:分别向三支试管中滴加5滴5%,2%,0.5%的酚酞溶液;(6)根据实验2和实验3可知,酚酞溶液浓度为0.5%,NaOH溶液的浓度为0.5%,酚酞试液不褪色;故答案为:0.5;(7)根据信息酚酞溶液由酚酞固体溶于酒精配制而成,因此要设计实验排除酒精对酚酞溶解的影响,故答案为:未排除酒精对酚酞溶解的影响.
答案:(1)分别向三支试管中滴加5滴5%,2%,0.5%的酚酞溶液(2)CO2+2NaOH=Na2CO3+H2O;(3)不成立;(4)与NaOH浓度有关,浓度过高会使酚酞褪色;(5)分别向三支试管中滴加5滴5%,2%,0.5%的酚酞溶液;(6)0.5(7)未排除酒精对酚酞溶解的影响.
(1)对整体实验分析可得出该空的结论(2)根据二氧化碳和氢氧化钠反应产生碳酸钠和水写出反应的发出;(3)根据实验现象分析结论;(4)根据表格的数据分析得出结论;(5)根据实验现象设计实验方案;(6)根据实验2和实验3分析现象及数据得出结论;(7)根据酚酞试液的配制过程分析可能的影响因素.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案