题目内容
【题目】请根据下列装置图回答问题: 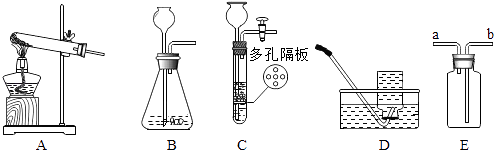
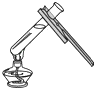
(1)若实验室用A装置制氧气,则反应的化学方程式为:;
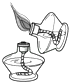
(2)装置B或装置C都可用来制二氧化碳,其中装置C的优点是:;
(3)常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体,易溶于水,水溶液则叫氢硫酸,密度比空气大,实验室常用硫化亚铁(FeS,固体)与稀硫酸发生复分解反应制得,反应的化学方程式为: , 若用E装置收集H2S气体,则H2S气体应从端通入(填a或b).
【答案】
(1)2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
(2)控制反应的发生与停止
(3)FeS+H2SO4=FeSO4+H2S↑;b
【解析】解:(1)实验室用A装置制氧气,由A装置的特点是加热固体制取气体且试管口没有棉花团,故所选的药品为氯酸钾和二氧化锰.加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气,其化学方程式为:2KClO3 ![]() 2KCl+3O2↑;故答案为:2KClO3
2KCl+3O2↑;故答案为:2KClO3 ![]() 2KCl+3O2↑;(2)由于装置C可以通过固体和液体的分离与结合来控制反应的发生与停止,而B装置中药品加入后,不能分离,一旦发生就不能控制;故C装置的优点是:控制反应的发生与停止;(3)硫化亚铁(FeS,固体)与稀硫酸发生复分解反应,由于复分解反应是两种化合物相互交换成分生成另外两种化合物的反应,故生成物为硫化氢和硫酸亚铁,故反应的化学方程式为:FeS+H2SO4=FeSO4+H2S↑;如果用E装置收集硫化氢气体,收集时应从b导管进入,由于硫化氢的密度比空气大,硫化氢沉积在集气瓶的底部,由下而上,充满集气瓶;故答案为:FeS+H2SO4=FeSO4+H2S↑ b. (1)由A装置的特点是加热固体制取气体且试管口没有棉花团,故所选的药品为氯酸钾和二氧化锰去分析;(2)由于装置C可以通过固体和液体的分离与结合来控制反应的发生与停止,而B装置中药品加入后,不能分离,一旦发生就不能控制;(3)硫化亚铁(FeS,固体)与稀硫酸发生复分解反应,由于复分解反应是两种化合物相互交换成分生成另外两种化合物的反应,故生成物为硫化氢和硫酸亚铁,如果用E装置收集硫化氢气体,收集时应从b导管进入.
2KCl+3O2↑;(2)由于装置C可以通过固体和液体的分离与结合来控制反应的发生与停止,而B装置中药品加入后,不能分离,一旦发生就不能控制;故C装置的优点是:控制反应的发生与停止;(3)硫化亚铁(FeS,固体)与稀硫酸发生复分解反应,由于复分解反应是两种化合物相互交换成分生成另外两种化合物的反应,故生成物为硫化氢和硫酸亚铁,故反应的化学方程式为:FeS+H2SO4=FeSO4+H2S↑;如果用E装置收集硫化氢气体,收集时应从b导管进入,由于硫化氢的密度比空气大,硫化氢沉积在集气瓶的底部,由下而上,充满集气瓶;故答案为:FeS+H2SO4=FeSO4+H2S↑ b. (1)由A装置的特点是加热固体制取气体且试管口没有棉花团,故所选的药品为氯酸钾和二氧化锰去分析;(2)由于装置C可以通过固体和液体的分离与结合来控制反应的发生与停止,而B装置中药品加入后,不能分离,一旦发生就不能控制;(3)硫化亚铁(FeS,固体)与稀硫酸发生复分解反应,由于复分解反应是两种化合物相互交换成分生成另外两种化合物的反应,故生成物为硫化氢和硫酸亚铁,如果用E装置收集硫化氢气体,收集时应从b导管进入.

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案【题目】在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参与反应且不溶于水)和纯碱为原材料制取烧碱,其制取流程如图: 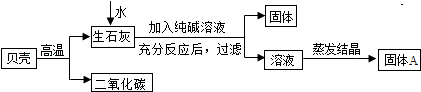
(1)写出加入纯碱溶液后发生反应的化学方程式:;
(2)[问题与发现]固体A是纯净的氢氧化钠吗? [猜想与假设]根据反应原理,同学们提出以下猜想:
甲的猜想:A是纯净的氢氧化钠固体.
乙的猜想:A是氢氧化钠和氢氧化钙的混合物.
你的猜想: .
[实验验证]
实验操作 | 现象 | 结论 | |
甲 | 取少量固体A,用适量水溶解后,滴加几滴无色酚酞溶液 | 溶液变红 | 猜想成立 |
乙 | 取少量固体A,用适量水溶解后,滴加几滴饱和碳酸钠溶液 | 猜想不成立 | |
你 | 猜想成立 |
[反思与评价]同学们讨论后,认为甲的结论不一定成立,原因是 .
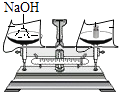
【题目】众所周知,酚酞溶液遇NaOH溶液变红.但是,在分组实验中(如图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物.
【提出问题】分组实验中,出现意想不到的现象的原因是什么呢?
【查阅资料】酚酞溶液由酚酞固体溶于酒精配制而成.
【猜想与假设】
Ⅰ.红色褪去,与NaOH溶液和空气中的CO2反应有关.
Ⅱ.红色褪去,与NaOH溶液的浓度有关.
Ⅲ.出现白色浑浊物,与酚酞溶液的浓度有关.
【进行实验】
实验 | 实验操作 | 实验现象 | |
1 | 向盛有2mL Na2CO3溶液的试管中 | 溶液变红 | |
2 |
| 1号试管0.1min红色褪去 | |
3 | 取3支试管,分别加入2mL水, . | 酚酞溶液浓度/% | 浑浊程度 |
5 | 大量浑浊物 | ||
2 | 少量浑浊物 | ||
0.5 | 无浑浊物 | ||
(1)补充上表中横线处内容:
(2)NaOH与CO2反应的化学方程式为 .
(3)实验1的现象表明,猜想与假设1(填“成立”或“不成立”).
(4)由实验2得出结论:出现“溶液变红后褪色”现象的原因是 .
(5)实验3的操作步骤:取3支试管,分别加入2mL水, .
(6)【反思与评价】依据现有实验,为了确保红色不变,若酚酞溶液浓度为0.5%,建议选用NaOH溶液的浓度为 %.
(7)有同学认为,仅通过实验3得出“猜想与假设Ⅲ成立”证据不足,理由是 .