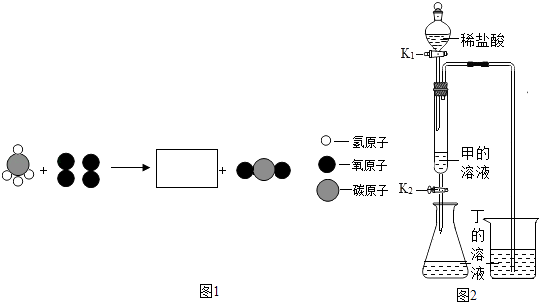
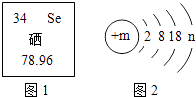
题目内容
【题目】如图实验操作正确的是( )
A. 稀释浓硫酸
稀释浓硫酸
B.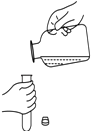 倾倒液体
倾倒液体
C.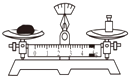 称量固体
称量固体
D.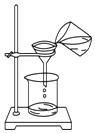 过滤
过滤
【答案】C
【解析】解:A、稀释浓硫酸时,由于水的密度较小,浮在浓硫酸上面,而浓硫酸溶于水时会放出大量的热,使水立刻沸腾,造成硫酸液滴向四周飞溅,这是非常危险的.因此,浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌,切不可将水倒进浓硫酸里.故A错误; B、倾倒液体时,容器口要与试管口紧挨,瓶塞要倒置,以防污染药品,故B错误;
C、使用托盘天平称量固体时,是“左物右码”,故C正确;
D、过滤时,缺少玻璃棒的引流,漏斗下端没有紧靠承接滤液的烧杯内壁,故D错误.
故选:C
【考点精析】关于本题考查的液体药品取用的方法和过滤操作的注意事项,需要了解液体药品的取用:①液体试剂的倾注法②液体试剂的滴加法;过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损才能得出正确答案.

【题目】众所周知,酚酞溶液遇NaOH溶液变红.但是,在分组实验中(如图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物.
【提出问题】分组实验中,出现意想不到的现象的原因是什么呢?
【查阅资料】酚酞溶液由酚酞固体溶于酒精配制而成.
【猜想与假设】
Ⅰ.红色褪去,与NaOH溶液和空气中的CO2反应有关.
Ⅱ.红色褪去,与NaOH溶液的浓度有关.
Ⅲ.出现白色浑浊物,与酚酞溶液的浓度有关.
【进行实验】
实验 | 实验操作 | 实验现象 | |
1 | 向盛有2mL Na2CO3溶液的试管中 | 溶液变红 | |
2 |
| 1号试管0.1min红色褪去 | |
3 | 取3支试管,分别加入2mL水, . | 酚酞溶液浓度/% | 浑浊程度 |
5 | 大量浑浊物 | ||
2 | 少量浑浊物 | ||
0.5 | 无浑浊物 | ||
(1)补充上表中横线处内容:
(2)NaOH与CO2反应的化学方程式为 .
(3)实验1的现象表明,猜想与假设1(填“成立”或“不成立”).
(4)由实验2得出结论:出现“溶液变红后褪色”现象的原因是 .
(5)实验3的操作步骤:取3支试管,分别加入2mL水, .
(6)【反思与评价】依据现有实验,为了确保红色不变,若酚酞溶液浓度为0.5%,建议选用NaOH溶液的浓度为 %.
(7)有同学认为,仅通过实验3得出“猜想与假设Ⅲ成立”证据不足,理由是 .