题目内容
①碱石灰是实验室常用的干燥剂,它是氧化钙、氢氧化钠的固体混合物. 除了能吸收水蒸气外,碱石灰还能吸收常见的气体是______(选填编号,只有一个答案,多选不得分).A.氧气 B.一氧化碳 C.二氧化碳 D.氢气
②实验室中利用草酸亚铁晶体受热分解得到一定量的 CO,反应的方程式 为:FeC2O4?2H2O→铁的氧化物+CO+CO2+2H2O该反应属于______(填写基本反应类型),根据质量守恒定律,可以推知产物中“铁的氧化物”的化学式是______
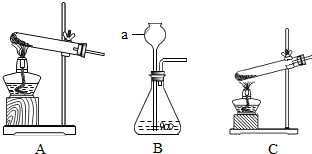
③加热草酸亚铁可选用下列“A、B、C”三套装置中的______(选填编号“A、B、C”).写出下列仪器“a”的名称是______.
④草酸亚铁晶体的摩尔质量是______(写全单位),若有1.8g 草酸亚铁晶体充分反应可得 到CO气体的物质的量是多少?请写出计算过程:
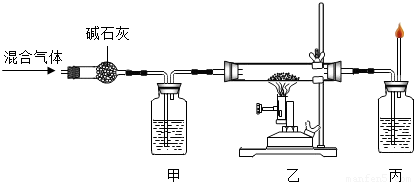
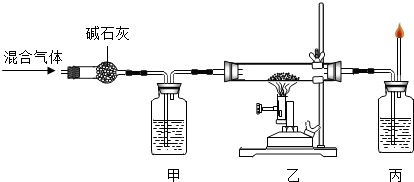
⑤草酸亚铁晶体受热分解得到的气体通过碱石灰后,用来与氧化铜反应,并检验反应得到的气体产物.整套装置如图:
写出“乙”处 反应的 现象是______,反应的 化学方程式 为______ Cu+CO2

【答案】分析:①碱石灰属于碱性干燥剂,可吸收酸性气体;
②根据反应特点和质量守恒定律定律推断物质的化学式;
③根据反应特点、反应条件和仪器的图形填空;
④根据化学方程式进行计算;
⑤混合气体中含有CO和CO2,CO具有还原性,能还原氧化铜,CO2能使澄清石灰水变浑浊,可据此分析.
解答:解:①碱石灰中的氢氧化钠能与二氧化碳、二氧化硫、氯化氢等气体反应,故可用来吸收酸性气体.
②从反应特点来看,反应物是一种,生成物是多种,属于分解反应,根据质量守恒定律,反应前后各元素的原子个数不变,故产物中“铁的氧化物”的化学式是 FeO.
③加热草酸亚铁固体生产气体,发生装置应选A,仪器“a”的名称是长颈漏斗.
④摩尔质量的数值和该物质的相对分子质量是一样的,根据草酸亚铁晶体的化学式(FeC2O4?2H2O),草酸亚铁晶体的摩尔质量是M=56+(12×2)+(16×4)+(2×18)=180克/摩尔,
设1.8g 草酸亚铁晶体充分反应可得到CO气体的质量为x:
FeC2O4?2H2O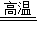 FeO+CO↑+CO2↑+2H2O
FeO+CO↑+CO2↑+2H2O
180 28
1.8g x
 x=0.28g
x=0.28g
生成的CO的物质的量为: =0.01mol
=0.01mol
⑤草酸亚铁晶体受热分解得到的气体通过碱石灰后,剩余的气体主要是CO,CO与氧化铜反应生成铜和二氧化碳,看到现象是黑色固体逐渐变红,反应的化学方程式为 CuO+CO Cu+CO2,该反应中还原剂是CO. 甲、丙两处所盛放的试液分别是澄清石灰水,其中“甲”处所盛放该试液的作用是检验并除去混合气体中的二氧化碳,以免影响实验结论,“丙”处的石灰水用来检验反应后生成的二氧化碳.
Cu+CO2,该反应中还原剂是CO. 甲、丙两处所盛放的试液分别是澄清石灰水,其中“甲”处所盛放该试液的作用是检验并除去混合气体中的二氧化碳,以免影响实验结论,“丙”处的石灰水用来检验反应后生成的二氧化碳.
故答案为:①C
②分解反应,FeO
③A,长颈漏斗
④180克/摩尔,0.01mol
⑤黑色固体逐渐变红,CuO+CO Cu+CO2,澄清石灰水、澄清石灰水,检验并除去混合气体中的二氧化碳,以免影响实验结论.
Cu+CO2,澄清石灰水、澄清石灰水,检验并除去混合气体中的二氧化碳,以免影响实验结论.
点评:此题综合性比较强,要在明确实验目的条件下,结合碱石灰、CO、CO2的性质进行分析解答,熟悉有关物质的量的计算,能准确利用化学方程式计算有关数据.
②根据反应特点和质量守恒定律定律推断物质的化学式;
③根据反应特点、反应条件和仪器的图形填空;
④根据化学方程式进行计算;
⑤混合气体中含有CO和CO2,CO具有还原性,能还原氧化铜,CO2能使澄清石灰水变浑浊,可据此分析.
解答:解:①碱石灰中的氢氧化钠能与二氧化碳、二氧化硫、氯化氢等气体反应,故可用来吸收酸性气体.
②从反应特点来看,反应物是一种,生成物是多种,属于分解反应,根据质量守恒定律,反应前后各元素的原子个数不变,故产物中“铁的氧化物”的化学式是 FeO.
③加热草酸亚铁固体生产气体,发生装置应选A,仪器“a”的名称是长颈漏斗.
④摩尔质量的数值和该物质的相对分子质量是一样的,根据草酸亚铁晶体的化学式(FeC2O4?2H2O),草酸亚铁晶体的摩尔质量是M=56+(12×2)+(16×4)+(2×18)=180克/摩尔,
设1.8g 草酸亚铁晶体充分反应可得到CO气体的质量为x:
FeC2O4?2H2O
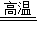 FeO+CO↑+CO2↑+2H2O
FeO+CO↑+CO2↑+2H2O180 28
1.8g x
 x=0.28g
x=0.28g生成的CO的物质的量为:
 =0.01mol
=0.01mol⑤草酸亚铁晶体受热分解得到的气体通过碱石灰后,剩余的气体主要是CO,CO与氧化铜反应生成铜和二氧化碳,看到现象是黑色固体逐渐变红,反应的化学方程式为 CuO+CO
 Cu+CO2,该反应中还原剂是CO. 甲、丙两处所盛放的试液分别是澄清石灰水,其中“甲”处所盛放该试液的作用是检验并除去混合气体中的二氧化碳,以免影响实验结论,“丙”处的石灰水用来检验反应后生成的二氧化碳.
Cu+CO2,该反应中还原剂是CO. 甲、丙两处所盛放的试液分别是澄清石灰水,其中“甲”处所盛放该试液的作用是检验并除去混合气体中的二氧化碳,以免影响实验结论,“丙”处的石灰水用来检验反应后生成的二氧化碳.故答案为:①C
②分解反应,FeO
③A,长颈漏斗
④180克/摩尔,0.01mol
⑤黑色固体逐渐变红,CuO+CO
 Cu+CO2,澄清石灰水、澄清石灰水,检验并除去混合气体中的二氧化碳,以免影响实验结论.
Cu+CO2,澄清石灰水、澄清石灰水,检验并除去混合气体中的二氧化碳,以免影响实验结论.点评:此题综合性比较强,要在明确实验目的条件下,结合碱石灰、CO、CO2的性质进行分析解答,熟悉有关物质的量的计算,能准确利用化学方程式计算有关数据.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
 33、碱石灰是实验室常用的干燥剂.
33、碱石灰是实验室常用的干燥剂.
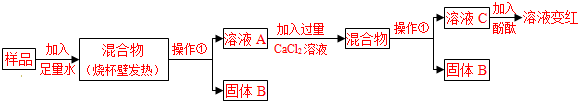
 碱石灰是实验室常用的干燥剂.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.
碱石灰是实验室常用的干燥剂.同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究.