题目内容
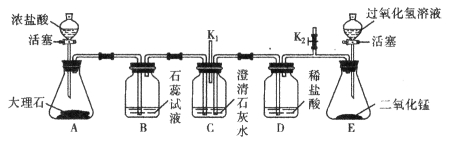
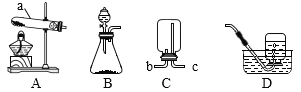
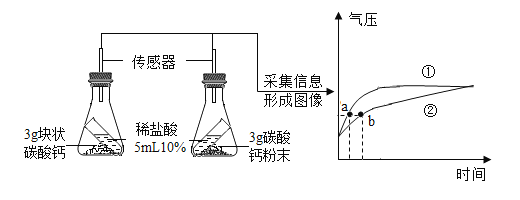
【题目】控制一定的温度,用图 1 装置在空气中焙烧 MnCO3 可以制取 MnO2。某探究学习小组查阅资料得知 MnCO3在空气中加热不同温度时易转化为锰的不同氧化物(锰元素的化合价有+2、+3、+4、+6、+7), 其残留固体质量随温度的变化如图 2 所示。下列说法正确的是

A.在空气中加热 MnCO3 发生的化学反应都属于分解反应
B.空气中焙烧 MnCO3 制取 MnO2,反应温度应控制在 900℃
C.a、b、c 三点所得锰的氧化物中锰元素的化合价越来越高
D.制取 MnO2 时在空气中焙烧 MnCO3是因为需氧气参加反应
【答案】D
【解析】
解:A、MnCO3在空气中加热时依次发生下列反应:
2MnCO3 2CO2+2MnO2
2CO2+2MnO2
4MnO2![]() 2Mn2O3+O2↑
2Mn2O3+O2↑
2Mn2O3![]() 4MnO+O2↑
4MnO+O2↑
故在空气中加热MnCO3发生的化学反应都属于分解反应,故正确;
B、设100g碳酸锰分解生成二氧化锰的质量为x,
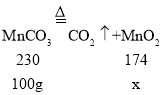
![]()
x≈75.65g,对应的温度为300℃,所以根据图可以看出,焙烧MnCO3制取MnO2应该控制反应的温度为300℃,故错误;
C、a点是二氧化锰,其中锰元素的化合价为+4,b点是Mn2O3,其中锰元素的化合价为+3,c点是MnO,其中锰元素的化合价为+2,故化合价越来越低,故错误;
D、由于加热过程中会生成MnO,所以装置内的空气提供的氧气能够使反应过程中转化为二氧化锰而不是MnO;所以焙烧时向石英管中通入空气的目的是 提供碳酸锰转化为二氧化锰的氧气,防止生成MnO,故错误。
故选D。

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目