题目内容
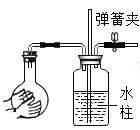
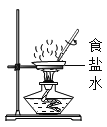
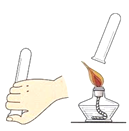
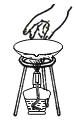
【题目】为验证“酸的化学通性”,某班同学在实验室进行了如下实验.请分析并回答相关问题:
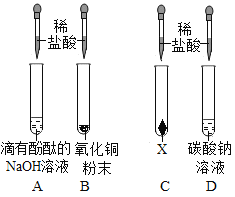
(1)写出能证明A中反应发生的现象__________;
(2)B中所发生的反应方程式为__________;
(3)要全面验证酸的化学通性,C试管中所放固体的物质类别为__________;
(4)D实验完成后,测得反应后的溶液pH=2,则该溶液中的溶质为__________.
【答案】溶液由红色变成无色 CuO+2HCl═CuCl2+H2O 金属 HCl、NaCl
【解析】
(1)盐酸和氢氧化钠反应后溶液呈中性,所以能证明A中反应发生的现象:溶液由红色变成无色;
(2)氧化铜和盐酸反应生成氯化铜和水,化学方程式为:CuO+2HCl═CuCl2+H2O;
(3)要全面验证酸的化学通性,C试管中所放固体的物质类别为金属;
(4)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,实验完成后,测得反应后的溶液pH=2,说明盐酸过量,所以该溶液中的溶质为:HCl、NaCl。
故答案为:(1)溶液由红色变成无色;
(2)CuO+2HCl═CuCl2+H2O;
(3)金属;
(4)HCl、NaCl。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目