题目内容
【题目】试管a、b中分别放入等质量的甲和乙,再分别加入等质量的水(析出固体不含结晶水)。
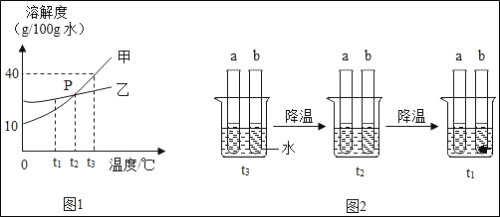
①t1℃时,甲的溶解度___乙的溶解度(用“>”“<”“=”填空)。
②p点的含义是___。
③图2,a中加入的物质是___(填“甲”或“乙”);
④t3℃时,若将25g甲物质加入到50g水中,充分溶解后得到溶液质量为___。
⑤关于图2说法中正确的是___。
A t1℃时a和b中溶剂质量相等
B t2℃时a和b均为不饱和溶液
C t3℃时a中溶质质量分数大于b中溶质质量分数
D t3℃时若使a和b均恰好饱和,a中加入对应溶质质量大于b中加入对应溶质质量
【答案】< t2℃时,甲、乙两种物质的溶解度相等 乙 70 AB
【解析】
①由图1可知,t1℃ 时,甲的溶解度曲线低于乙的溶解度曲线,所以t1℃ 时,甲的溶解度小于乙的溶解度,故填<。
②由图1可知,t2℃ 时,价、乙两物质的溶解度曲线相较于P点,则P点的含义是t2℃时,甲、乙两种物质的溶解度相等,故填t2℃时,甲、乙两种物质的溶解度相等。
③由图2可知,将等质量的甲和乙,再分别加入等质量的水中充分溶解,固体均溶解,降低温度后,试管a中无晶体析出,试管b中有晶体析出,说明试管a中的物质的溶解度受温度影响较小,试管b中的物质的溶解度受温度影响较大,所以试管a 中加入的物质是图1中的物质乙,故填乙。
④由图1可知,t3℃ 时,物质甲的溶解度为40g,即t3℃ 时,100g水中最多溶解甲40g,t3℃ 时,若将 25g 甲物质加入到 50g 水中,充分溶解后只有20g甲溶解,得到溶液质量为70g,故填70。
⑤A由题文试管 a、b 中分别放入等质量的甲和乙,再分别加入等质量的水可知,两支试管中的溶剂质量相等,降温至t1℃ 时,溶剂不变,所以 a 和 b 中溶剂质量相等,选项正确;
B 温度降至t1℃ 时,试管a中就没有析出晶体,说明t2℃ 时 a 中的溶液为不饱和溶液;降温至t3℃ 时 b 试管才析出晶体,说明t2℃ 时 b 中的溶液也为不饱和溶液,选项正确;
C t3℃ 时,试管 a、b 中分别放入等质量的甲和乙,再分别加入等质量的水,两支试管中均没有固体剩余,所以a 中溶质质量分数等于 b 中溶质质量分数,选项错误;
D 由③可知,试管a 中加入的物质是乙,且t3℃ 时乙的溶解度小于甲的溶解度,所以t3℃ 时若使 a 和 b 均恰好饱和,a 中加入对应溶质质量小于 b 中加入对应溶质质量,选项错误,故填AB。

【题目】某化学兴趣小组同学往NaOH溶液中滴加无色酚酞溶液时,发现溶液变成红色,可是过了一会儿红色消失,重新恢复为无色。于是该小组在老师指导下对这一现象进行了探究。
(提出问题)溶液的红色为什么会变成无色呢?
(猜想与假设)
猜想一:可能是所用的酚酞溶液变质了
猜想二:可能是NaOH与空气中的CO2反应了
猜想三:可能是酚酞与空气中的O2反应了
猜想四:可能是与NaOH溶液浓度大小有关
(查阅资料)Na2CO3俗称纯碱,是一种发酵剂, Na2CO3溶液的pH值通常约为10~11.9
(讨论交流)
(1)写出氢氧化钠在空气中变质的化学方程式:__________ 。
(2)对于猜想一,大家认为是错误的。往氢氧化钠溶液中滴加酚酞溶液时,发现溶液变成了红色,说明所用酚酞没变质。
(3)小组同学集体讨论后认为猜想二 ______(填“合理”或“不合理”),原因是______。
(设计并实验)
(1)为了验证猜想三,小组同学进行了如下实验:先向如图装有该NaOH溶液的试管中,从b处通入密度比空气大的稀有气体,将试管内的空气排尽。然后通过注射器滴入无色酚酞溶液,观察到溶液变成红色,过一会儿红色仍然消失。则猜想三______(填“正确”或“错误”)。

(2)为了验证猜想四,小组同学继续进行实验探究,并得出了实验结论,请你帮助该小组完成下表:
实验操作 | 实验现象 | 实验结论 |
在两支同样大小的试管中,分别加入等体积的质量分数为5%的氢氧化钠溶液和10%的氢氧化钠溶液,然后分别滴加1﹣2滴酚酞试液; | 5%的氢氧化钠溶液中红色不消失,10%的氢氧化钠溶液中先变红色,然后红色消失 | 猜想四__ (填“正确”或“错误”) |
(拓展延伸)
小组同学百度“酚酞”得知,酚酞(用H2In表示)其实是一种极弱的酸,遇碱溶液变红的变化可表示为:H2In(无色)![]() In2-(红色),据此信息写出H2In遇NaOH溶液变红的化学反应方程式为_____________。
In2-(红色),据此信息写出H2In遇NaOH溶液变红的化学反应方程式为_____________。