题目内容
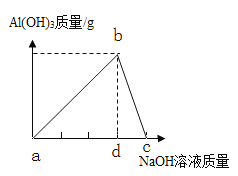
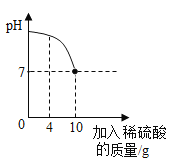
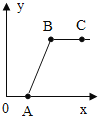
【题目】废液缸中剩有大量的稀盐酸与氯化钙的混合溶液(不考虑其他杂质),某同学取上层清液于烧杯中,逐滴滴入Na2CO3溶液至过量。记录滴入Na2CO3溶液质量(x)与有关量的变化关系如图所示。下列判断正确的是( )
A.C点溶液的![]()
B.图中纵坐标![]() 表示生成
表示生成![]() 的质量
的质量
C.反应进行到A点时,溶液中的溶质是NaCl和![]()
D.OA段发生反应的化学方程式是![]()
【答案】C
【解析】
A、实验探究进行到C点时,反应早已经结束,因为过量的碳酸钠溶液加入其中,溶液的pH大于7,故错误;
B、根据碳酸钠与稀盐酸和氯化钙的混合溶液的反应原理,向混合溶液中逐滴滴入Na2CO3溶液至过量,相比之下,刚开始是稀盐酸的量多,而碳酸钠的量少,溶液中应先冒气泡,而不是先产生沉淀。所以,图中纵坐标(y)应该表示生成的沉淀质量,故错误;
C、从开始反应的O点到A点的OA段,发生了如下的化学反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,反应进行到A点时,溶液中的溶质是NaCl和未参加反应的氯化钙,故正确;
D.从开始反应的O点到A点的OA段,发生了如下的化学反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,故错误。
故选C。

练习册系列答案
相关题目