题目内容
【题目】金属钴和锰及它们的化合物用途广泛,请根据题目回答。
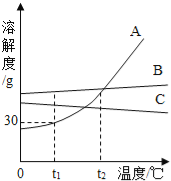
(1)部分锰的化合物的颜色及溶解性见下表:
物质 | KMnO4 | MnO2 | MnO | Mn3O4 | MnSO4 | MnCO3 |
颜色 | 黑色 | 黑色 | 绿色 | 黑色 | 白色 | 白色 |
溶解性 | 易溶 | 难溶 | 难溶 | 难溶 | 易溶 | 难溶 |
①上述固体中,显绿色的是_____。
②若向 MnSO4 溶液的试管中滴入 Na2CO3 溶液,化学方程式是_____。
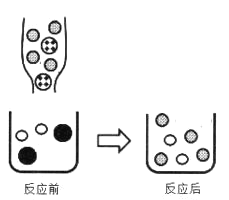
③下图表示上述反应前后溶液中存在的主要离子,写出以下图形代表的离子:______、______
![]()
(2)已知 Co2O3 固体黑色粉末,CoSO4 溶液是粉红色的。向盛有 Co2O3 的试管里加入稀硫酸, 发生反应 2Co2O3+4H2SO4===4CoSO4+O2↑+4H2O。预设观察到的现象是______
【答案】![]()
![]()
![]()
![]() 黑色粉末消失,溶液变成红色,溶液有气泡冒出
黑色粉末消失,溶液变成红色,溶液有气泡冒出
【解析】
由表格可以看出锰的化合物的颜色及溶解性,MnSO4 溶液和 Na2CO3 溶液反应生成硫酸钠和碳酸锰沉淀。
①固体中,显绿色的是![]() 。
。
②MnSO4 溶液和 Na2CO3 溶液反应生成硫酸钠和碳酸锰沉淀,向 MnSO4 溶液的试管中滴入 Na2CO3 溶液,化学方程式是![]() 。
。
③反应前后溶液中存在的主要离子是![]() 和
和![]() 。
。
(2)Co2O3 固体黑色粉末,CoSO4 溶液是粉红色的,向盛有 Co2O3 的试管里加入稀硫酸, 发生反应 2Co2O3+4H2SO4===4CoSO4+O2↑+4H2O,观察到的现象是黑色粉末消失,溶液变成红色,溶液有气泡冒出。

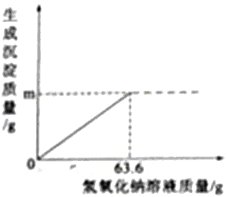
【题目】纯碱产品中常含有少量的氯化钠杂质,在实验室中取50g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为30g),每次充分反应后都进行称量,得到的实验数据如表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入纯碱样品的质量/g | 10 | 10 | 10 | 10 | 10 |
电子天平的示数/g | 137.8 | a | 153.4 | 161.2 | 171.2 |
(1)a的值为_____。
(2)计算纯碱样品中碳酸钠的质量_____。
(3)计算所用稀盐酸的溶质质量分数_____。
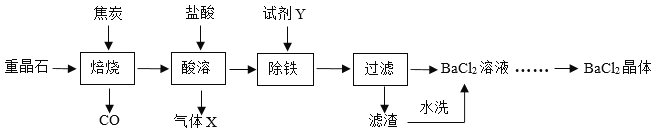
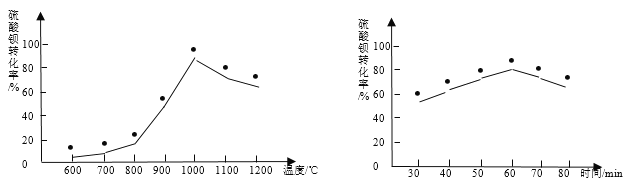
【题目】某兴趣同学在实验室的试剂柜中发现一瓶失去标签的无色溶液,可能是硫酸、 硝酸铁、氯化钠、氢氧化钡中的其中一种。为了确定该无色溶液并预测其化学性质, 进行下列实验:
(1)根据上述信息判断,该溶液一定不是________________溶液。(填化学式,下同)
(2)取样,用 pH 试纸测定该溶液呈碱性,该溶液一定是________________溶液。
(3)请预测其化学性质,说出预测依据,并设计实验验证。 限用试剂:酚酞溶液、铁、盐酸、氧化铜、硫酸钾溶液、硝酸镁溶液、硝酸铜溶液。
预测 | 预测的依据 | 检验预测的实验操作与预测现象 |
(1)能与含有 | 氢氧化钡溶液能解离 出 | 取少量待测溶液于试管中,滴入________________溶液,如果观察到________________则预测成立。 |
(2)能与_______________(填物质类别)反应 | _______________ | 取 少 量 待 测 溶 液 于 试 管 中 ,__________ , 如果观察到 _________ _, 则预测成立。 |