题目内容
【题目】下图是某同学绘制的四种实验数据的变化趋势图象,其中正确的是( )
A. 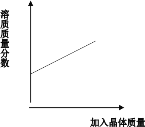 某温度下,向一定量接近饱和的氯化钠溶液中不断加入氯化钠晶体
某温度下,向一定量接近饱和的氯化钠溶液中不断加入氯化钠晶体
B.  向等质量的金属镁和铁中分别滴加足量且溶质质量分数相等的稀硫酸
向等质量的金属镁和铁中分别滴加足量且溶质质量分数相等的稀硫酸
C.  用等质量、等浓度的双氧水分别制取氧气
用等质量、等浓度的双氧水分别制取氧气
D.  碳在密闭容器(含有空气)内燃烧,容器内元素种类随时间的变化情况
碳在密闭容器(含有空气)内燃烧,容器内元素种类随时间的变化情况
【答案】D
【解析】
A、向一定量接近饱和的氯化钠溶液中不断加入氯化钠晶体,氯化钠不断溶解,溶质质量分数不断增大,氯化钠溶液达到饱和后,氯化钠溶液的溶质质量分数不变,故A错误;
B、根据化学化学方程式Mg + H2SO4 = MgSO4 + H2↑,Fe + H2SO4 = FeSO4 + H2↑可知,每24份质量的镁生成2份质量的氢气,每56份质量的铁生成2份质量的氢气。向等质量的金属镁和铁中分别滴加足量且溶质质量分数相等的稀硫酸,完全反应后,镁生成的氢气多,图像与之不符,故B错误;
C、用等质量、等浓度的双氧水分别制取氧气,生成氧气的质量相同,与催化剂无关,故C错误;
D、由元素守恒可知,碳在密闭容器(含有空气)内燃烧,容器内元素种类不变,故D正确。故选D。

【题目】化学实验技能是学习化学和进行探究活动的基础和保证。以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究:
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:____________。
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转 |
结论 | 猜想1正确 | 猜想2正确 反应的化学方程式为:__________________ |
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转.得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在中_________进行.
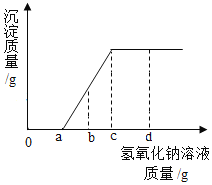
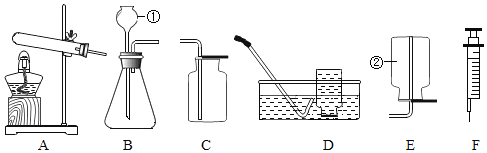
(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是____________。
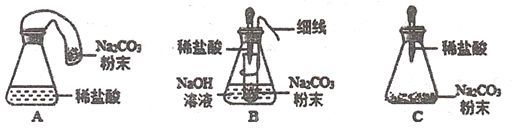
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_____________的各物质的质量总和等于反应后生成的各物质的质量总和。
(解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:硝酸铵(NH4NO3)固体在不同温度下发生不同的分解反应,则下列各物质不可能是该反应产物的是__________(填序号)
A.NH3 B.H2O C.SO2 D.N2
【题目】某同学为测定黄铜屑(由锌和铜形成的合金)样品组。分四次取样品与稀盐酸反应,其实验数据记录见下表。
1 | 2 | 3 | 4 | |
取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
试计算:
①第几次实验金属锌完全反应________。
②所用稀硫酸中溶质的质量分数_______?