题目内容
【题目】水是人类赖以生存的物质之一,也是实验室最常用的物质之一。
(1)下列含“水”的物质属于纯净物的是_____(填字母序号)。
A 自来水 B 冰水混合物 C 河水 D 蒸馏水
(2)明矾是常用的净水剂之一,其作用是_____;用明矾净化后的水是_____(填“软水”或“硬水”);高铁酸钾(K2FeO4)也可用来净化水, K2FeO4中铁元素的化合价为_____。制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,则X的化学式为_____。
(3)为了防止水的污染,下列做法有利于保护水资源的是_____ (填编号)。
①抑制水中所有动、植物的生长 ②不任意排放工业废水 ③大量使用化肥农药 ④生活污水经过净化处理后再排放
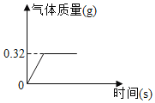
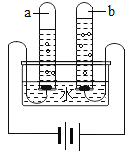
(4)如图是简易的电解水实验示意图。其中b管产生的气体为_____,反应的化学方程式为_____;晓明同学用自制电解器电解水,在水中加少许硫酸钠,目的是_____;当他在103.6g质量分数为5%的硫酸钠溶液中通电一段时间后,产生3.2 g氧气,此时另一极产生的氢气质量为_____;配制5%的硫酸钠溶液用到的玻璃仪器有烧杯、玻璃棒、_____,此时,硫酸钠的质量分数为_____(精确到0.01%)。
【答案】BD 吸附较大颗粒,加速沉降 硬水 +6 KCl ②④ 氧气 2H2O![]() 2H2↑+O2↑ 增强水的导电性 0.4g 漏斗 5.18%
2H2↑+O2↑ 增强水的导电性 0.4g 漏斗 5.18%
【解析】
解:(1)冰水混合物、蒸馏水都是由一种物质组成的属于纯净物;在自来水、河水中含有可溶、不可溶性的杂质,属于混合物;
(2)明矾是常用的净水剂之一,其作用是吸附较大颗粒、加速沉降;根据化合价代数和为0的原则可知,高铁酸钾中Fe显+6价;根据反应的化学方程式:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,反应物中铁、氧、钾、氢、氯原子个数分别为2、16、10、16、6,反应后的生成物中铁、氧、钾、氢、氯原子个数分别为2、16、4、16、0,根据反应前后原子种类、数目不变,则6X中含有6个钾原子和6个氯原子,则每个X分子由1个钾原子和1个氯原子构成,则物质X的化学式为KCl;
(3))①抑制水中所有动植物的生长,不能保持生态平衡,不能防止水污染,故错误;
②不任意排放污水和对污水先处理再排放有利于保护水资源,故正确;
③大量使用化肥农药,能够引起水体污染,不利于保护水资源,故错误;
④生活污水经过净化处理后再排放,能够减少水污染,有利于保护水资源,故正确;
(4)接通直流电源一段时间后,玻璃管a内产生的气体较多,是氢气,玻璃管b内产生的气体较少,是氧气,反应的化学方程式为2H2O![]() 2H2↑+O2↑;在水中加少许硫酸钠,目的是增强水的导电性;设生成3.2g氧气时同时生成的氢气的质量为x,
2H2↑+O2↑;在水中加少许硫酸钠,目的是增强水的导电性;设生成3.2g氧气时同时生成的氢气的质量为x,

![]()
x=0.4g;
配制5%的硫酸钠溶液用到的玻璃仪器有烧杯、玻璃棒、漏斗;
电解后溶液中硫酸钠的质量分数为:![]() ×100%=5.18%。
×100%=5.18%。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____________。
(查阅资料)CaC12 滚液显中性
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想I:只有CaC12
猜想II:有__________
猜想III:有CaC12和Ca(OH)2
猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_________。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
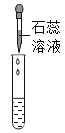
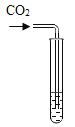
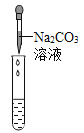
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ____________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想III是正确的。
(评价反思) (1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________。
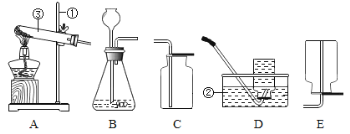
【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实 验 装 置 |
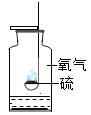
硫在氧气中燃烧 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氢气 (氢气难溶于水) |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察氢气何时收集满 |
A.AB.BC.CD.D
【题目】某学生为了探究甲烷的组成元素,设计并完成了如下探究实验,请你帮他完成下面的实验报告:
提出问题:甲烷中含有哪些元素?
(查阅资料)含碳元素的物质完全燃烧生成![]() 。
。
实验探究:
实验步骤 | 实验现象 | 解释与结论 |
①在空气中点燃甲烷, ②将洁净干燥的小烧杯罩在甲烷燃烧的火焰上方。 | 烧杯内壁有水珠。 | 证明生成物有水,甲烷中一定含有_______元素。 |
③将蘸有澄清石灰水的小烧杯罩在甲烷燃烧的火焰上方。 | _____________。 | 证明生成物有 |
(1)表达与交流:经实验测定甲烷的化学式为![]() ,请你写出甲烷燃烧方程式:________________。
,请你写出甲烷燃烧方程式:________________。
【题目】实验室常用氯酸钾或过氧化氢溶液抽取氧气,现提供下图装置进行实验,回答问题:
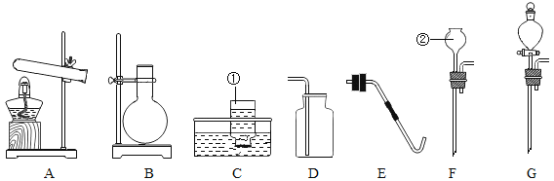
(1)写出编号仪器的名称①__________;②__________。
(2)实验室用氯酸钾和二氧化钙的混合物制取并收集较纯净的氧气,可选择的装置组合为________(填字母),二氧化锰在该反应中做______,实验结束时撤装置,应进行的操作是________;A装置中试管口略向下倾斜的目的是________。
(3)为了得到稳定的气流,实验室用过氧化氢溶液制取氧气应选择_________(填字母)组合成发生装置;若用向上排气法收集氧气,检验氧气集满的方法是:__________。导气管深入集气瓶底部是为了________。
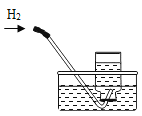
(4)若用下图装置进行“排空气法”收集制取H2,请把图中的“导气管”补画完整。________

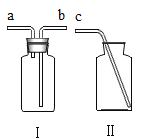
(5)常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2═2NO2)。为了收集纯净的NO气体,利用下图所示仪器Ⅰ、Ⅱ。用胶管将___________(填导管口字母)与c相连组成收集装置。收集时应先在Ⅰ中________________。
(6)要验证氧气中混有二氧化碳和水蒸气,可选下列装置_________进行验证。

(7)取氯酸钾和二氧化锰的混合物60g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表:
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
剩余固体质量/g | 5.1 | 4.5 | 4.2 | 4.08 | 4.08 | 4.08 |
①.生成氧气的质量为_________g
②.求原混合物中二氧化锰的质量________?(根据化学方程式写计算)