题目内容
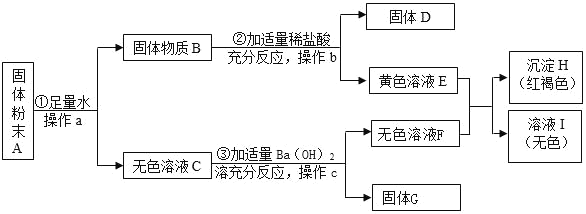
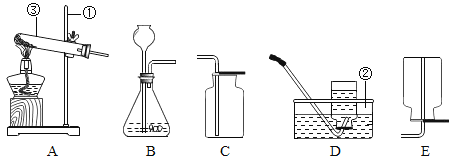
【题目】实验室常用氯酸钾或过氧化氢溶液抽取氧气,现提供下图装置进行实验,回答问题:
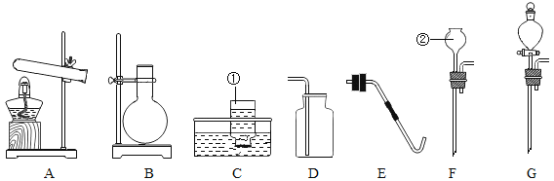
(1)写出编号仪器的名称①__________;②__________。
(2)实验室用氯酸钾和二氧化钙的混合物制取并收集较纯净的氧气,可选择的装置组合为________(填字母),二氧化锰在该反应中做______,实验结束时撤装置,应进行的操作是________;A装置中试管口略向下倾斜的目的是________。
(3)为了得到稳定的气流,实验室用过氧化氢溶液制取氧气应选择_________(填字母)组合成发生装置;若用向上排气法收集氧气,检验氧气集满的方法是:__________。导气管深入集气瓶底部是为了________。
(4)若用下图装置进行“排空气法”收集制取H2,请把图中的“导气管”补画完整。________

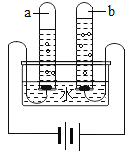
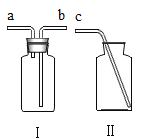
(5)常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2═2NO2)。为了收集纯净的NO气体,利用下图所示仪器Ⅰ、Ⅱ。用胶管将___________(填导管口字母)与c相连组成收集装置。收集时应先在Ⅰ中________________。
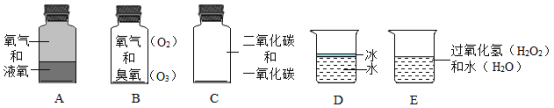
(6)要验证氧气中混有二氧化碳和水蒸气,可选下列装置_________进行验证。

(7)取氯酸钾和二氧化锰的混合物60g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表:
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
剩余固体质量/g | 5.1 | 4.5 | 4.2 | 4.08 | 4.08 | 4.08 |
①.生成氧气的质量为_________g
②.求原混合物中二氧化锰的质量________?(根据化学方程式写计算)
【答案】集气瓶 长颈漏斗 ACE 催化剂 将导管移出水面 防止冷凝水回流使试管炸裂 BG 将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了 充分排出集气瓶内的空气 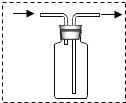 b 装满水 甲 1.92 1.1g
b 装满水 甲 1.92 1.1g
【解析】
(1)仪器①是集气瓶,仪器②是长颈漏斗;故填:集气瓶;长颈漏斗;
(2)如果用氯酸钾和二氧化锰制氧气就需要加热,其中二氧化锰起催化作用;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;实验结束时撤装置,应进行的操作是将导管移出水面;A装置中试管口略向下倾斜的目的是防止冷凝水回流使试管炸裂;
故答案为:ACE;催化剂;将导管移出水面;防止冷凝水回流使试管炸裂;
(3)如果用双氧水和二氧化锰制氧气就不需要加热,分液漏斗可以控制反应的速率,应选择BG组合成发生装置;若用向上排气法收集氧气,氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;导气管深入集气瓶底部是为了充分排出集气瓶内的空气。
故答案为:BG;将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;充分排出集气瓶内的空气;
(4)因H2的密度比空气的密度小,因此收集时,要短管进,长管出;
故答案为: ;
;
(5)题目已经给出NO的有关信息:难溶于水的气体,密度比空气略大,因此最好使用排水法,Ⅰ中就必须装满水,要使得Ⅰ中的水排干净,就必须用b连接c。故选B 装满水;
故答案为:b;装满水;
(6)要验证氧气中混有二氧化碳和水蒸气,可以用无水硫酸铜检验水,澄清石灰水检验二氧化碳,但是水必须先检验。
故选:甲;
(7)①根据质量守恒定律生可知生成氧气的质量为:6.0g-4.08g=1.92g;
②设原混合物中氯酸钾的质量为x

解得:x=4.9g
原混合物中二氧化锰的质量=6.0g-4.9g=1.1g
答:原混合物中二氧化锰的质量为1.1g。