题目内容
高温加热碳酸钙可制得生石灰和二氧化碳,现高温加热10g碳酸钙,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%。此时反应生成的二氧化碳质量为
| A.4.4克 | B.2克 | C.2.4克 | D.4克 |
B
解析试题分析:根据钙元素的质量在反应前后守恒解题。
首先求出10g碳酸钙中含钙元素多少克,过程如下:10g×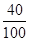 ×100%=4g
×100%=4g
其次,由于钙元素守恒,反应后固体中钙元素仍为4g,则反应后固体质量为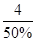 =8g。
=8g。
最后,生成二氧化碳为10-8=2g
考点:质量守恒定律应用

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案
相关题目
工业上以CaO和HNO3为原料制备Ca(NO3)2?6H2O晶体.为确保制备过程中既不补充水,也无多余的水,所用硝酸的溶质质量分数约为
| A.41.2% | B. 53.8% | C.58.3% | D.70.0% |
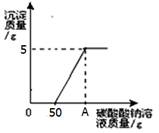
向溶质的质量分数为17%的硝酸银溶液中逐滴滴入稀盐酸,测得滴入盐酸的质量与生成沉淀的质量有如图所示关系,则恰好完全反应时所得溶液中溶质的质量分数为
| A.6.3% | B.7.3% | C.10% | D.17% |
将17.4g部分变质的氢氧化钙,加入到200g7.3%的稀盐酸中,恰好完全反应,则所得溶液中溶质的质量为
| A.11.1g | B.14.2g | C.22.2g | D.44.4g |
电解水时,常在水中加入氢氧化钠使反应容易进行,氢氧化钠本身并不被分解.现用118g溶质质量分数为10%的氢氧化钠溶液进行电解水的实验,一段时间后,溶液中溶质质量分数变为11.8%,下列数据计算正确的是( )
| A.产生氧气质量为8g | B.溶液中氢氧化钠质量为18g |
| C.被电解的水的质量为18g | D.反应后溶液质量为90g |
在某H2O2溶液中氢元素与氧元素的质量比为2:17,现向19g该H2O2溶液中加入1g二氧化锰,充分反应后,生成氧气的质量为
( )
| A.1g | B.1.6g | C.4.2g | D.8.5g |