题目内容
【题目】碳酸锂作为锂的基础锂盐,广泛用于玻璃制造和陶瓷生产过程中的添加剂,也是制备锂电池的重要原料。碳酸锂在热水中的溶解度很小,工业上以锂辉石精矿(主要成分是Li2O、含有Al2O3、SiO2等杂质)为原料制取碳酸锂的硫酸法生产工艺流程如下
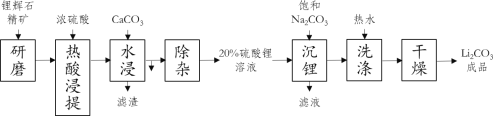
(1)锂辉石热酸浸提前要进行“研磨”,其目的是_____
(2)“水浸”中加入CaCO3的作用之一是为了调节pH=5,让溶液中的Al3+变成Al(OH)3沉淀出来,要确定溶液的pH值为5,可以用pH试纸来测定,其操作方法是_____
(3)“沉锂”中加入的Na2CO3溶液是饱和溶液,其作用是_____,反应的化学方程式为_____
(4)“洗涤”中使用热水,原因是_____,证明洗涤干净的方法是_____
(5)为了探究热酸浸提的最佳条件,将矿石在一定条件下酸浸4小时,锂元素浸出率的数据如下表
编号 | 矿酸比 | 硫酸浓度(%) | MgSO4用量(g) | 温度(℃) | 锂元素浸出率(%) |
1 | 1:1 | 90 | 0.00 | 100 | 70.34 |
2 | 1:1 | 98 | 0.00 | 100 | 73.89 |
3 | 1:1 | 98 | 0.00 | 150 | 78.24 |
4 | 1:3 | 98 | 0.00 | 200 | 85.53 |
5 | 1:3 | 98 | 1.25 | 250 | 90.26 |
6 | 1:3 | 98 | 2.50 | 250 | 95.88 |
①本实验中,编号为_____两组实验能说明温度对锂元素浸出率的影响
②根据上表数据,MgSO4用量对锂元素浸出率的影响是_____
③在工业生产过程中,相当数量的硫酸和纯碱变成了价值较低的Na2SO4等物质,从而造成了生产成本的提高,为了降低生产成本,除了尽可能减少硫酸的配量外,降低能源消耗也是一个方面,因此,可以继续设计实验,以探究出最佳锂元素浸提工艺条件,下列设计合理的是_____(填字母)
A 矿酸比1:2,硫酸浓度98,MgSO4用量0.00,温度150℃
B 矿酸比1:2,硫酸浓度98,MgSO4用量1.25,温度200℃
C 矿酸比1:2,硫酸浓度98,MgSO4用量2.50,温度200℃
D 矿酸比1:2,硫酸浓度98,MgSO4用量2.50,温度250℃
【答案】增大矿物与酸的接触面积,加快热酸浸提的速率 将一小片pH试纸放在白瓷板上,用干燥玻璃棒蘸取溶液滴到pH试纸上,再与标准比色卡比对,读出pH 提高反应物的浓度,有利于Li2SO4转化为Li2CO3 Li2SO4+Na2CO3==Na2SO4+Li2CO3↓ 碳酸锂在热水中溶解度很小,避免了洗涤过程中碳酸锂的损耗 取少量洗涤后的溶液于试管中,滴入足量稀盐酸,充分反应后滴入氯化钡溶液,若无明显现象,则已洗涤干净 2和3 其他条件相同时,增大MgSO4的用量,锂元素的浸出率提高 CD
【解析】
(1)锂辉石要粉碎成细颗粒的目的是增加接触面积,使反应充分,加快热酸浸提的速率;
(2)用pH试纸来测定,其操作方法是:将一小片pH试纸放在白瓷板上,用干燥玻璃棒蘸取溶液滴到pH试纸上,再与标准比色卡比对,读出pH;
(3)加入Na2CO3溶液是饱和溶液可以提供浓度大的溶液,可以使Li2SO4转化为Li2CO3;硫酸锂和碳酸钠反应生成硫酸钠和碳酸锂沉淀,反应的化学方程式为:Li2SO4+Na2CO3=Na2SO4+Li2CO3↓;
(4)由表中数据可知:温度越高,锂元素浸出率越高;由此可知,用热水的原因是:碳酸锂在热水中溶解度很小,避免了洗涤过程中碳酸锂的损耗;可以验证洗涤后的溶液中含有碳酸根离子,不含硫酸根离子即可,方法为:取少量洗涤后的溶液于试管中,滴入足量稀盐酸,充分反应后滴入氯化钡溶液,若无明显现象,则已洗涤干净;
(5)①对比表中数据可知:2和3两组实验能说明温度对锂元素浸出率的影响;
②根据上表数据可知:其他条件相同时,增大MgSO4的用量,锂元素的浸出率提高;
③其他条件相同时,MgSO4的用量越大,锂元素的浸出率提高,可知方法合理的是CD。