题目内容
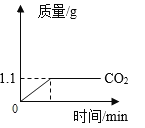
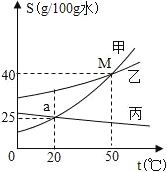
【题目】向一密闭容器中加入甲、乙、丙、丁 4 种物质,在一定条件下发生化学反应,测得有关数据如图,下列说法不正确的是( )
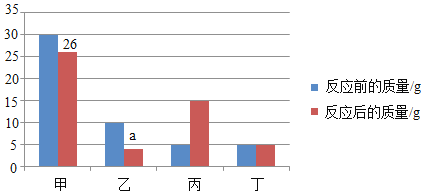
A.a 的数值是 4
B.丙一定属于化合物
C.参加反应的乙和丙的质量比为 3∶5
D.丁一定是该反应的催化剂
【答案】D
【解析】
由表中数据分析可知,反应前后甲的质量减少了30g-26g=4g,故是反应物,参加反应的质量为4g;同理可以确定丙是生成物,生成的质量为15g-5g=10g;丁的质量不变,可能作该反应的催化剂,也可能没有参加反应;由质量守恒定律,乙应是反应物,且参加反应的质量为10g-4g=6g,故a的数值为10g-6g=4g。
A、由上述分析,a的数值是4,故选项说法正确。
B、该反应的反应物为甲和乙,生成物是丙,符合“多变一”的形式,属于化合反应,丙是化合反应的生成物,一定属于化合物,故选项说法正确。
C、参加反应的乙和丙的质量比为6g:10g=3:5,故选项说法正确。
D、丁的质量不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法错误。
故选:D。

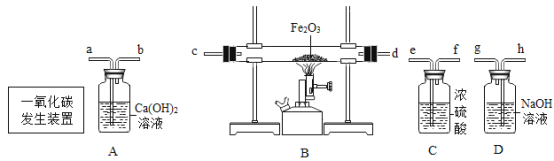
【题目】1775年法国化学家拉瓦锡用定量的方法研究了空气的成分。仿照这个历史上著名实验的原理,如今我们的化学教育家积极探索、不断创新,先后设计出了如图所示的实验装置。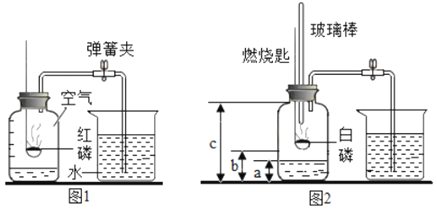
(提出问题)用红磷燃烧的方法为什么测出的氧气含量远低于21%?
(分析讨论)(1)实验装置漏气;(2)______,导致装置内氧气有剩余;(3)……
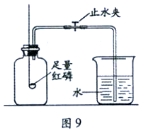
(实验改进)(1)如图2所示的实验装置进行实验探究。实验前在集气瓶里先装进a体积的水,其作用:一是为了加快集气瓶的冷却速度;二是______。
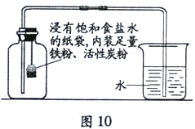
(2)如图3所示的实验装置进行实验探究。
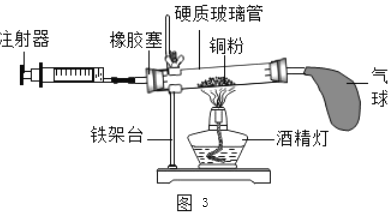
①在实验过程中,不断推拉注射器的目的是______。
②写出该实验中反应的化学方程式______。
③测得实验结果如下(气体体积):(单位:mL)
反应前玻璃管内 | 反应前注射器内 | 反应后注射器内 |
40 | 30 | 18 |
由此数据可以推算出他测定的空气中氧气的体积分数为______。
(实验结论)(1)研究空气的成分实验是在密封容器内进行。
(2)该物质在空气中可以燃烧且只与空气中的氧气反应。
(3)燃烧后的产物______。