题目内容
【题目】某同学对酸碱盐的知识进行了以下梳理
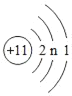
(1)请根据下表盐中的金属元素的排列顺序,填写空格中的化学式:
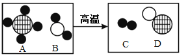
KNO3 | Ca(NO3)2 | Na(NO3)2 | Mg(NO3)2 | _____。 | Zn(NO3)2 | Fe(NO3)2 |
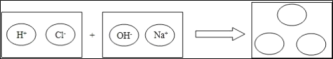
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在如图的圆圈中填入适当的化学式或离子符号应该是_____.
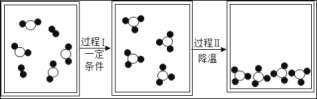
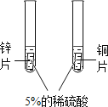
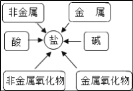
(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,①、②中任选一个,写出反应的化学方程式:_____.
【答案】Al(NO3)3 H2O,Na+,Cl﹣ Fe+CuSO4═FeSO4+Cu(或Fe2O3+3H2SO4═Fe2(SO4)3+3H2O)
【解析】
(1)由表表格盐中金属的活动性顺序和盐的组成可知,应填物质的盐为硝酸铝,化学式是:Al(NO3)3;
(2)稀盐酸和氢氧化钠两者反应的微观实质,氢离子与氢氧根离子生成水,氯离子和钠离子存在于水溶液中,故可知图片中要填的答案为:H2O,Na+,Cl﹣;
(3)①用稀硫酸除铁锈的化学方程式Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
②古代记载“曾青得铁则化为铜”(“曾青”是指硫酸铜溶液)的化学方程式:Fe+CuSO4═FeSO4+Cu
故答为:(1)AlCl3;金属的活动性;(2)图片中要填的答案为 H2O,Na+,Cl﹣;
(3)Fe+CuSO4═FeSO4+Cu(或Fe2O3+3H2SO4═Fe2(SO4)3+3H2O).

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把40g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),充分反应后经过过滤、干燥等操作,最后称量,得实验数据如下:
次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸质量/g | 10 | 10 | 10 | 10 |
剩余固体的质量/g | 3.0 | 2.0 | 1.2 | m |
则求:⑴在第____次反应稀盐酸开始出现剩余,反应停止进行;上表格表m= ______g;
⑵求该石灰石样品中碳酸钙的质量分数为_______;
⑶实验室现要制取二氧化碳气体9.24克,需要上述这种纯度的石灰石质量为_____________?(要求有计算过程)
【题目】空气中氧气含量测定的再认识:
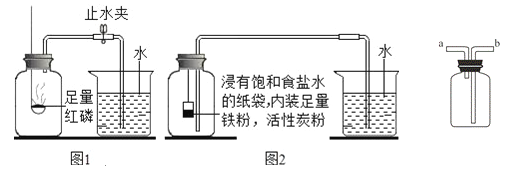
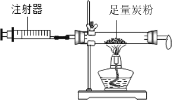
【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的文字表达式: 。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内 减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大。
【实验改进】
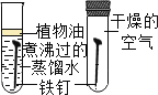
Ⅰ、根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量。装置中的饱和食盐水、活性炭会加速铁生锈。
Ⅱ、测得实验数据如下表:
测量项目 | 实验前 | 实验后 | |
烧杯中水的 体积 | 烧杯中剩余的 体积 | 集气瓶(扣除内容物)和导管的 容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
【交流表达】(1)铁生锈过程中发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的文字表达式: 。
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是 (计算结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
① ;② 。