题目内容
一气体混合物中含有CO2、CO、H2O和N2四种气体.现将其分别通过如下试剂(均足量),请判断所得气体的组成情况(假设每步反应都进行完全).
(1)依次通过NaOH溶液、浓H2SO4,最后得到的气体有 (填化学式).写出发生反应的化学方程式
(2)依次通过灼热的氧化铜粉末、浓H2SO4,最后得到的气体有: (填化学式).写出发生反应的化学方程式 .
(3)依次通过灼热的氧化铜粉末、NaOH溶液、浓H2SO4,最后得到的气体有: (填化学式).
(1)依次通过NaOH溶液、浓H2SO4,最后得到的气体有
(2)依次通过灼热的氧化铜粉末、浓H2SO4,最后得到的气体有:
(3)依次通过灼热的氧化铜粉末、NaOH溶液、浓H2SO4,最后得到的气体有:
考点:气体的净化(除杂),书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯
分析:根据NaOH溶液、浓H2SO4、灼热的氧化铜的特性来考虑,氢氧化钠溶液能吸收酸性气体,浓硫酸具有吸水性,炽热的氧化铜能与还原性气体反应.
解答:解:(1)通过NaOH溶液把二氧化碳反应掉了,通过浓H2SO4把水蒸气吸收了,最后得到的气体有一氧化碳和氮气;
(2)通过炽热的氧化铜时一氧化碳与其反应,吸收了一氧化碳,生成了二氧化碳;然后通过浓H2SO4把水蒸气吸收了,最后得到的气体有二氧化碳和氮气.
(3)通过炽热的氧化铜时一氧化碳与其反应,吸收了一氧化碳,生成了二氧化碳;通过NaOH溶液把二氧化碳反应掉了,通过浓H2SO4把水蒸气吸收了,最后得到的气体为氮气;
故答案为:(1)CO、N2 2NaOH+CO2=Na2CO3+H2O
(2)CO2、N2 CO+CuO
Cu+CO2
(3)N2
(2)通过炽热的氧化铜时一氧化碳与其反应,吸收了一氧化碳,生成了二氧化碳;然后通过浓H2SO4把水蒸气吸收了,最后得到的气体有二氧化碳和氮气.
(3)通过炽热的氧化铜时一氧化碳与其反应,吸收了一氧化碳,生成了二氧化碳;通过NaOH溶液把二氧化碳反应掉了,通过浓H2SO4把水蒸气吸收了,最后得到的气体为氮气;
故答案为:(1)CO、N2 2NaOH+CO2=Na2CO3+H2O
(2)CO2、N2 CO+CuO
| ||
(3)N2
点评:通过回答本题可知NaOH溶液能除去二氧化碳、浓H2SO4除去水、炽热的氧化铜粉末能除去一氧化碳.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列材料中属于有机合成材料的是( )
| A、不锈钢 | B、水泥 | C、涤纶 | D、羊毛 |
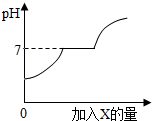 常温下,许多盐如CaCl2、NaCl等物质的水溶液呈中性.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
常温下,许多盐如CaCl2、NaCl等物质的水溶液呈中性.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )| A、纯净水 | B、澄清的石灰水 |
| C、碳酸钠溶液 | D、稀盐酸 |
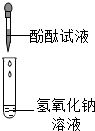 同学们在探究碱的化学性质时,发现了一个意外现象,向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.
同学们在探究碱的化学性质时,发现了一个意外现象,向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.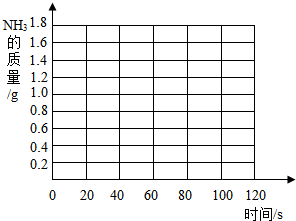 某校科学兴趣小组为测定某样品中氯化铵的质量分数,将6g样品溶于18g水后,再加入7.6g氢氧化钠浓溶液共热,两者恰好完全反应(样品中的杂质不与氢氧化钠反应,也不溶于水,氯化铵与氢氧化钠的反应方程式为:NH4Cl+NaOH
某校科学兴趣小组为测定某样品中氯化铵的质量分数,将6g样品溶于18g水后,再加入7.6g氢氧化钠浓溶液共热,两者恰好完全反应(样品中的杂质不与氢氧化钠反应,也不溶于水,氯化铵与氢氧化钠的反应方程式为:NH4Cl+NaOH