题目内容
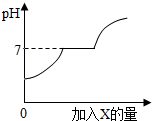 常温下,许多盐如CaCl2、NaCl等物质的水溶液呈中性.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
常温下,许多盐如CaCl2、NaCl等物质的水溶液呈中性.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )| A、纯净水 | B、澄清的石灰水 |
| C、碳酸钠溶液 | D、稀盐酸 |
考点:酸的化学性质,溶液的酸碱性与pH值的关系,盐的化学性质
专题:常见的酸 酸的通性,常见的盐 化学肥料
分析:根据当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性等知识进行分析.
解答:解:由图可以看出,当加入X物质时,遇到盐酸会反应,之后随着盐酸的消耗,加入物质能够与氯化钙反应,但是对应生成物必须是中性的,而继续加入X,溶液显碱性,所以加入物质不能是碱,但是却显碱性.
A、HCl与CaCl2的混合溶液显酸性,加入水时溶液的pH升高,只能逐渐的接近7,但是不会等于或大于7,故A错误;
B、加入石灰水时,氢氧化钙能和盐酸反应生成氯化钙和水,溶液的pH升高,当酸完全被消耗之后,继续滴加石灰水,由于和氯化钙不反应,所以pH值马上大于7,而不会出现水平等于7的一段,故B错误;
C、加入纯碱溶液时,碳酸钠能和盐酸反应,也能和氯化钙反应.开始时碳酸钠和盐酸反应,导致pH上升;当酸完全被消耗时,碳酸钠和氯化钙反应,生成物都是中性的,一直到氯化钙被完全消耗;当继续滴加碳酸钠时,由于碳酸钠显碱性,所以pH大于7,故C正确;
D、加入盐酸时,盐酸和氯化钙不反应,溶液的pH不能等于或大于7,故D错误.
故选:C.
A、HCl与CaCl2的混合溶液显酸性,加入水时溶液的pH升高,只能逐渐的接近7,但是不会等于或大于7,故A错误;
B、加入石灰水时,氢氧化钙能和盐酸反应生成氯化钙和水,溶液的pH升高,当酸完全被消耗之后,继续滴加石灰水,由于和氯化钙不反应,所以pH值马上大于7,而不会出现水平等于7的一段,故B错误;
C、加入纯碱溶液时,碳酸钠能和盐酸反应,也能和氯化钙反应.开始时碳酸钠和盐酸反应,导致pH上升;当酸完全被消耗时,碳酸钠和氯化钙反应,生成物都是中性的,一直到氯化钙被完全消耗;当继续滴加碳酸钠时,由于碳酸钠显碱性,所以pH大于7,故C正确;
D、加入盐酸时,盐酸和氯化钙不反应,溶液的pH不能等于或大于7,故D错误.
故选:C.
点评:本题主要考查了溶液的酸碱性和溶液pH的关系方面的知识,同时考查了读图能力,从图中提炼解题的关键要素.

练习册系列答案
相关题目
水是人类生活中不可缺少的物质.下列关于水的说法中不正确的是( )
| A、水是生命活动不可缺少的物质 |
| B、水通电分解和水的蒸发都是化学变化 |
| C、用肥皂水可以检验硬水和软水 |
| D、净化水的方法有吸附、沉淀、过滤等 |
X、Y、Z、W是四种不同的金属,为比较它们的活动性强弱,某同学利用这四种金属单质、稀盐酸、Z的硝酸盐溶液、W的硝酸盐溶液,进行有关实验,结果如下表(能发生置换反应的记为“√”,不能反应的记为“一”,无标记的表示未做该实验).这四种金属的活动性顺序为( )
| X | Y | Z | W | |
| 盐酸 | √ | - | - | √ |
| Z的硝酸盐 | √ | |||
| W的硝酸盐 | √ | - |
| A、X>Y>W>Z |
| B、X>W>Y>Z |
| C、W>X>Y>Z |
| D、Y>W>Z>X |
生活中处处有化学.以下过程只发生物理变化的是( )
| A、将氮肥硝酸铵和熟石灰混放会降低肥效 |
| B、用醋酸除去热水瓶内壁上的水垢 |
| C、被蚊子叮咬后涂抹肥皂水止痛 |
| D、冰箱内放入活性炭除去异味 |
下列四个坐标图分别表示四个实验过程中某些量的变化,其中能正确反映其对应操作中各量变化关系的是( )
A、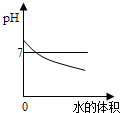 向pH=12的氢氧化钠溶液中不断加水 |
B、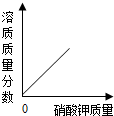 向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 |
C、 加热一定质量的高锰酸钾 |
D、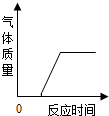 在部分变质的NaOH溶液中加稀盐酸 |
目前市场上出现的木糖醇(化学式为C5H12O5)是一种新型甜味剂,它不能被细菌分解,添加在口香糖里取代糖分,可防止蛀牙.下列关于木糖醇的说法正确的是( )
| A、木糖醇中含有5个碳原子、12个氢原子和5个氧原子 |
| B、木糖醇中碳、氢、氧元素的质量比为5:12:5 |
| C、木糖醇中氢元素的质量分数最大 |
| D、木糖醇由碳、氢、氧三种元素组成 |
 小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧生成氧化铝(Al2O3),于是设计了如右图所示的装置进行实验探究,请你结合实验过程回答下列问题.(1)集气瓶底预先铺少量沙子的目的是
小强同学经过查阅资料得知:铝丝和铁丝一样,也能在氧气中燃烧生成氧化铝(Al2O3),于是设计了如右图所示的装置进行实验探究,请你结合实验过程回答下列问题.(1)集气瓶底预先铺少量沙子的目的是