题目内容
【题目】能源、环境与人类的生活和社会发展密切相关。
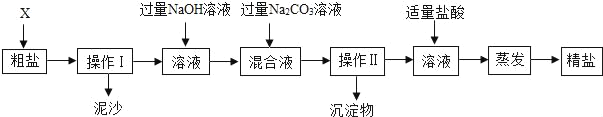
(1)目前,人类以化石燃料为主要能源,化石燃料是_____(选填“可再生”或“不可再生”)能源;
(2)随着工业生产的高速发展和人们生活水平的不断提高,人类所消耗的化石能源急剧增加,由此对环境造成的不良影响主要有_____(限举两例);所以我们要践行简约适度、绿色低碳的生活方式。
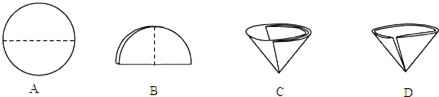
(3)汽车三元催化器中发生一个重要的反应,可减少有害气体排放,其反应过程的微观变化如图所示,反应前后的四种物质中属于单质的是_____(填化学式)。
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
【答案】不可再生 酸雨、温室效应 N2
【解析】
化石燃料有煤、石油和天然气,单质是由同种元素组成的纯净物。
(1)化石燃料有煤、石油和天然气,由于它们生成时间很长,都属于不可再生能源。
(2)化石燃料燃烧产生的二氧化碳会导致温室效应,产生的二氧化硫会形成酸雨。
(3)单质有同种分子构成,且该分子中只含有一种原子,故D属于单质,其化学式为N2。

 金钥匙试卷系列答案
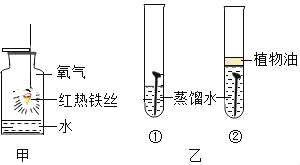
金钥匙试卷系列答案【题目】根据资料报道,世界上每年因锈蚀而报废的金属设备和材料相当于年产量的20%~40%,某实验小组对铁的锈蚀进行了如下探究.如图所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
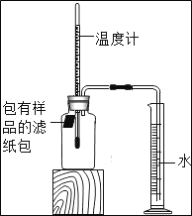
序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
① | 1g铁粉、0.2g碳和十滴水 | 100 | 72 | 约120 |
② | 1g铁粉、0.2g碳、十滴水和少量NaCl | 100 | 72 | 约70 |
③ | _____ | / | / | / |
(1)金属腐蚀的过程实际上就是金属元素化合价_____(填“升高”或“降低”)的过程.
(2)实验①和②说明NaCl可以_____(填“加快”或“减慢”)铁锈蚀的速率.
(3)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程.
(4)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____.
(5)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____.
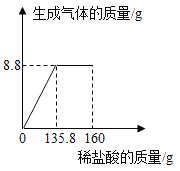
(6)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____%(精确到0.1%).试分析该实验结果出现误差的原因:_____(写出任意一条即可).
【题目】化学小组同学在某工厂废水处理池中提取一瓶含有AgNO3、Cu(NO3)2和Al(NO3)3的工业废水样品带回实验室。静置,取上层清液,加入锌粉,充分反应后过滤,得到滤液甲和滤渣乙。请完成以下探究(不考虑杂质干扰)。
(提出问题)滤渣乙是什么?
(做出猜想)小明认为滤渣乙是银,小东认为滤渣乙是银和铜,小华认为滤渣乙是银、铜和铝,你认为滤渣乙还可能是_____。
(交流讨论)大家经过讨论后,认为小华的猜想错误,理由是_____。
(实验探究)设计实验探究滤渣乙的成分,请填写下列空白:
实验步骤 | 现象 | 结论 |
步骤1:取滤渣乙加入盐酸 | 无气体产生 | 滤渣乙可能是_____ |
步骤2:取滤液甲插入打磨过的铁丝 | 无明显现象 | 滤渣乙一定是_____ |
(反思交流)通过交流,大家认为此时滤液甲中含有的溶质是_____。