题目内容
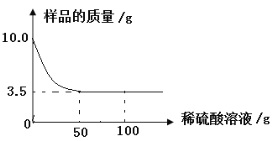
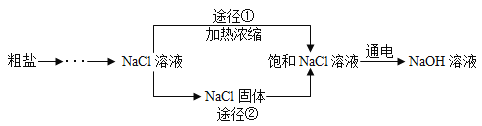
【题目】某混合物中含有氯化钠和碳酸钠,为测定碳酸钠的质量分数,某小组同学进行了如图实验,请计算:

(1)生成二氧化碳的总质量为 。
(2)样品中碳酸钠的质量分数(计算结果精确至0. 1%)。
【答案】4.4g、88.3%
【解析】
(1)碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,第一次加入50g稀盐酸,生成二氧化碳的质量为:12g+50g-59.8g=2.2g,第二次加入60g稀盐酸,生成二氧化碳的质量为:59.8g+60g-117.6g=2.2g,说明第二次加入60g稀盐酸,碳酸钠已经完全反应,生成二氧化碳的总质量为:2.2g+2.2g=4.4g;
(2)设样品中碳酸钠的质量分数为x
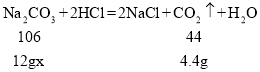
![]() x≈88.3%
x≈88.3%
答:样品中碳酸钠的质量分数为88.3%。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目