题目内容
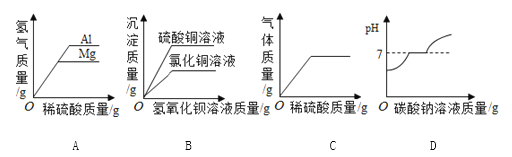
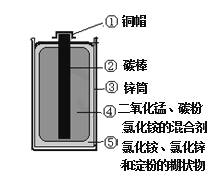
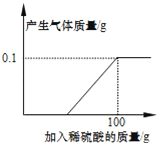
【题目】硫酸锌片在医药方面可用于治疗食欲不振、发育不良等症状,实验室可用锌和稀硫酸反应制得.学校化学兴趣小组的同学取一块表面严重氧化的锌片7.3g(不含其它杂质),剪碎,向其中慢慢滴加9.8%的稀硫酸,至恰好完全反应时,用去稀硫酸100g,并绘出如图所示的图象.小组同学将反应后的溶液经一系列操作,得到硫酸锌16.1g.
(1)小组同学在老师的指导下,配制200g 9.8%的稀硫酸.
①用98%的浓硫酸配制200g 9.8%的稀硫酸,需加水__g.
②将配制好的稀硫酸转移到试剂瓶中,贴上标签,标签上必须注明的是___(填序号).
A.200g B.9.8% C.稀硫酸
③下列操作中的___(填序号),可能会导致配制的溶液的溶质的质量分数低于9.8%.
A.量取浓硫酸后,置于空气中时间过长 B.量水时,俯视量筒刻度
C.配制前将烧杯用水冲洗干净,没有擦干
(2)生成0.1g氢气消耗的稀硫酸的质量是_____;
(3)该锌片没有氧化前的质量是____g.
【答案】 180g BC AC 50g 6.5
【解析】(1)①用98%的浓硫酸配制200g9.8%的稀硫酸,需加水的质量为:200g![]() =180g;②试剂瓶上需要注明药品的名称和溶质质量分数,故选:BC;③导致配制的溶液的溶质的质量分数低于9.8%的可能原因是溶质少了或溶剂多了,A、量取浓硫酸后,置于空气中时间过长,导致浓硫酸的质量减少了,所以溶质质量分数偏低,正确;B、量水时,俯视量筒刻度,水的体积少了,导致溶质质量分数偏大,错误;C、配制前将烧杯用水冲洗干净,没有擦干,导致溶剂的质量多了,所以溶质质量分数偏低,正确,故选:AC;(2)设生成0.1g氢气消耗的稀硫酸的质量是x
=180g;②试剂瓶上需要注明药品的名称和溶质质量分数,故选:BC;③导致配制的溶液的溶质的质量分数低于9.8%的可能原因是溶质少了或溶剂多了,A、量取浓硫酸后,置于空气中时间过长,导致浓硫酸的质量减少了,所以溶质质量分数偏低,正确;B、量水时,俯视量筒刻度,水的体积少了,导致溶质质量分数偏大,错误;C、配制前将烧杯用水冲洗干净,没有擦干,导致溶剂的质量多了,所以溶质质量分数偏低,正确,故选:AC;(2)设生成0.1g氢气消耗的稀硫酸的质量是x
Zn+H2SO4=ZnSO4+H2↑
98 2
x×9.8% 0.1g
![]() ,x=50g;(3)锌和硫酸反应生成硫酸锌和氢气,氧化锌和硫酸反应生成硫酸锌和水,所以依据硫酸根离子守恒可知,设该锌片没有氧化前的质量是y
,x=50g;(3)锌和硫酸反应生成硫酸锌和氢气,氧化锌和硫酸反应生成硫酸锌和水,所以依据硫酸根离子守恒可知,设该锌片没有氧化前的质量是y
ZnH2SO4,
65 98
y 100g×9.8%
![]() ,y=6.5g。
,y=6.5g。

【题目】分析处理图表信息是学习的一种重要方法。下表是氯化钠和硝酸钾在不同温度下的溶解度。
温度/℃ | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 36.0 | 36.6 | 37.3 | 38.4 |
KNO3 | 31.6 | 63.9 | 110 | 169 | |
这两种固体物质在水中的溶解度曲线如图所示:
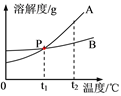
请仔细阅读图表后回答下列问题:
(1)A曲线表示的是________的溶解度曲线。(填“NaCl”或“KNO3”)
(2)P点的含义是___________________________。
(3)t2℃时,将等质量的A和B的饱和溶液降温至t1℃,所得溶液的质量大小关系是A____B。(填“<”、“>”或“=”)