题目内容
【题目】请根据下列装置回答问题:
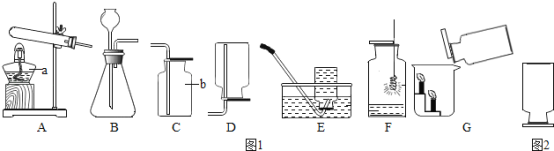
(1)写出标号仪器名称:a_____;b_____.
(2)实验室用高锰酸钾制取氧气时,发生装置应选用_____(填字母),其反应的化学方程式为_____,二氧化锰是该反应的_____,
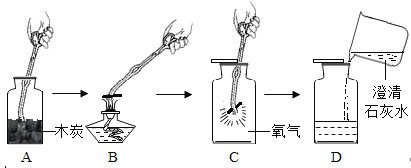
(3)实验室制取二氧化碳时,选择的药品是_____和_____,发生装置最好选用_____(填字母,下同),收集装置选用_____;B装置中长颈漏斗的作用_____写出实验室制取二氧化碳的化学方程式_____.二氧化碳气体用澄清石灰水进行检验,写出化学方程式_____.
(4)如果选择与制取CO2相同的发生装置来制取O2,则化学方程式为_____,其基本反应类型是_____.
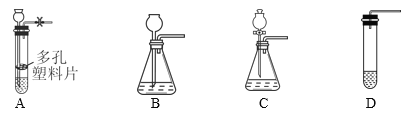
(5)实验室收集某气体只能用装置D,由此说明该气体具有的物理性质_____.
(6)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择_____(填序号).甲烷气体一般采用装置E进行收集,收集满后集气瓶的放置方式如图2所示,据此可推断甲烷一定具备的物理性质是:_____、_____.
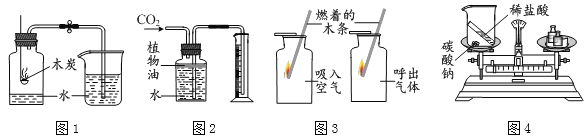
(7)收集一瓶二氧化碳,供G 实验使用,将二氧化碳倒入烧杯中,观察到的实验现象是_____,该实验说明二氧化碳具有的物理性质是_____;化学性质是_____.
(8) F瓶是铁丝在氧气中燃烧的实验,集气瓶底部水的作用_____.
【答案】酒精灯 集气瓶 A 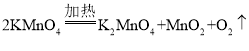 生成物 石灰石或者大理石 稀盐酸 B C 添加液体药品
生成物 石灰石或者大理石 稀盐酸 B C 添加液体药品 ![]()
![]()
![]() 分解反应 密度比空气小、易溶于水 A 难溶于水 密度比空气小 下面蜡烛先熄灭,上面蜡烛后熄灭 密度比空气大 不能燃烧也不支持燃烧 防止高温溅落物使瓶底炸裂
分解反应 密度比空气小、易溶于水 A 难溶于水 密度比空气小 下面蜡烛先熄灭,上面蜡烛后熄灭 密度比空气大 不能燃烧也不支持燃烧 防止高温溅落物使瓶底炸裂
【解析】
(1)标号仪器名称分别为:a酒精灯;b集气瓶。
(2)实验室用加热高锰酸钾的方法制取氧气,属于固体加热型,发生装置应选用A,加热高锰酸钾反应生成锰酸钾、二氧化锰和氧气,其反应的化学方程式为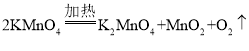 ,二氧化锰是该反应的生成物。
,二氧化锰是该反应的生成物。
(3)实验室制取二氧化碳时,选择的药品是石灰石或者大理石和稀盐酸,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,该反应属于固液混合不需加热型,发生装置最好选用B,二氧化碳密度比空气大、能溶于水并与水反应,收集装置选用C;B装置中长颈漏斗的作用是添加液体药品,实验室制取二氧化碳的化学方程式为![]() ;二氧化碳气体用澄清石灰水进行检验,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为
;二氧化碳气体用澄清石灰水进行检验,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为![]() 。
。
(4)如果选择与制取二氧化碳相同的发生装置来制取氧气,则是二氧化锰催化过氧化氢反应生成水和氧气的反应,则化学方程式为![]() ,符合“一变多”特征,其基本反应类型是分解反应。
,符合“一变多”特征,其基本反应类型是分解反应。
(5)实验室收集某气体只能用装置D,只能用向下排空法,不能用排水法,由此说明该气体具有的物理性质是密度比空气小、易溶于水。
(6)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择A,甲烷气体一般采用装置E即排水法进行收集,收集满后集气瓶的放置方式如图2所示倒放,据此可推断甲烷一定具备的物理性质是:难溶于水、密度比空气小。
(7)收集一瓶二氧化碳,供G 实验使用,将二氧化碳倒入烧杯中,观察到的实验现象是下面蜡烛先熄灭,上面蜡烛后熄灭,该实验说明二氧化碳具有的物理性质是密度比空气大;化学性质是不能燃烧也不支持燃烧。
(8)F瓶用于进行铁在氧气中燃烧的实验,瓶底水的作用是防止高温溅落物使瓶底炸裂。

 阅读快车系列答案
阅读快车系列答案【题目】探究水的元素组成:
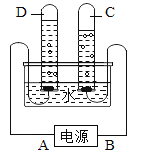
①图一是电解水的实验装置,电源A是______极,试管D中的气体是_______。
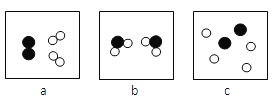
②图二是氢气燃烧的微展示意图,反应过程的正确顺序是_________(用a、b、c表示)。
从该图可以体现化学变化的实质是________。
|
|
图一:电解水 | 图二:氢气燃烧 |
③以上两个实验都可以得出实验结论:_____________。
④实验
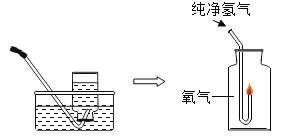
氢气在氧气中燃烧 | 步骤一 制取一瓶氧气 步骤二 纯净的氢气在这瓶氧气中燃烧
现象:氢气燃烧,发出____色火焰,瓶壁发热 | 该实验不能达到实验目的的原因是__________________ |
【题目】石灰石常见的矿产之一。学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数(石灰石中所含的杂质既不溶于水也不与稀盐酸反应),取来了10克的矿石样品,并取稀盐酸80 g,平均分成4份,依次加入进行4次实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
矿石样品质量/g | 10 | 10 | 10 | 10 |
稀盐酸质量/g | 20 | 40 | 60 | 80 |
生成CO2的质量/g | 0.88 | 1.76 | 2.2 | m |
(1)上表中m的数值是_________;
(2)试计算这种石灰石矿中碳酸钙的质量分数______。(写出计算过程)