题目内容
【题目】石灰石常见的矿产之一。学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数(石灰石中所含的杂质既不溶于水也不与稀盐酸反应),取来了10克的矿石样品,并取稀盐酸80 g,平均分成4份,依次加入进行4次实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
矿石样品质量/g | 10 | 10 | 10 | 10 |
稀盐酸质量/g | 20 | 40 | 60 | 80 |
生成CO2的质量/g | 0.88 | 1.76 | 2.2 | m |
(1)上表中m的数值是_________;
(2)试计算这种石灰石矿中碳酸钙的质量分数______。(写出计算过程)
【答案】2.2 50%(详见解析)
【解析】
(1)根据实验结果数据表,20g稀盐酸完全反应可以生成二氧化碳0.88g,若60g稀盐酸完全反应生成二氧化碳质量=0.88g×3=2.64g,而实验中仅放出2.2g二氧化碳,说明此时稀盐酸没有完全反应,石灰石中的碳酸钙完全消耗,盐酸没有完全反应是由于石灰石不足;所以第四次实验石灰石仍然不足,m为2.2;
(2)设:石灰石中碳酸钙的质量为x,则根据实验3中酸剩余,可得:
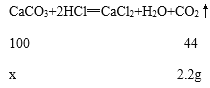
![]() x═5g;
x═5g;
石灰石矿中碳酸钙的质量分数=![]() 。
。
答:这种石灰石中碳酸钙的质量分数为50%。

 阅读快车系列答案
阅读快车系列答案【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式________________________________________。
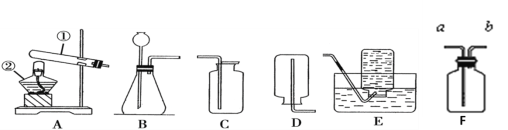
(2)小兵用下图装置收集并测量氢气的体积,其中量筒的作用是_______________________,氢气应从________(填e或f或g)管通入。

【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】
(4)结论是___________________________________________。
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。
_____________________________________。